 EndoTODAY 내시경 교실
EndoTODAY 내시경 교실
Beginner | ESA | Schedule | OPD
Seminars | Atlas | Recent | Links
 [Helicobacter pylori negative gastric cancer (HPNGC). 헬리코박터 음성 위암] - 終
[Helicobacter pylori negative gastric cancer (HPNGC). 헬리코박터 음성 위암] - 終
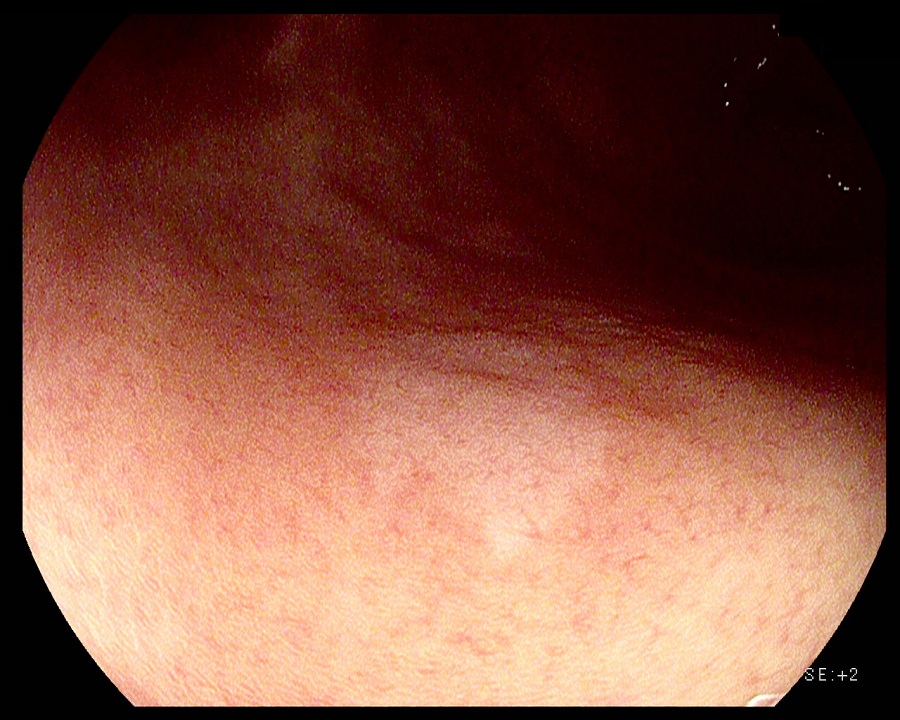
조직검사는 signet ring cell carcinoma였으며 ESD로 치료하였고 5mm lamina propria cancer였음.
1. 2017년 한일 내시경학회. Sugano 선생님 조찬 강의
2. 2017년 내시경학회 세미나. 송경호 교수님 강의
5. FAQs
6. References
 1. 2017년 한일 내시경학회 Sugano 선생님 조찬 강의
1. 2017년 한일 내시경학회 Sugano 선생님 조찬 강의
학회 때마다 breakfast session은 꼭 참석하는 편입니다. 그런데 이번 학회만큼 breakfast session이 대성황을 이룬 것은 본 적이 없습니다. 대단한 시간이었습니다.
Hp negative gastric cancer는 두 종류가 있습니다. (1) GC arising in the Hp-uninfected mucosa (familial GC, EBV-associated GC, autoimmune gastritis-associated GC, sporadic cancer with unknown causes)와 (2) GC arising in the mucosa infected with Hp in the past (spontaneous disappearance - advanced atrophy/IM, post-eradication therapy)
Hp 음성을 정의하는 것은 간단한 일이 아닙니다. Current infection 뿐만 아니라 past infection도 있으며 모든 검사가 일정한 정도의 false negative를 가지고 있기 때문입니다. 다른 모든 검사에서 음성이고 단지 CagA 항체만 양성인 경우도 있습니다.
Hp 감염이 한번도 없었던 환자의 위암은 최근 리뷰에서는 1.7% 정도였습니다 (Yamamoto Y. Digest Endosc 2015). Genuine Hp - gastric cancer는 1% 미만일 것으로 생각됩니다. 이 비율은 검사를 얼마나 strict하게 하는가에 따라 달라집니다. 예를 들어 CagA 항체 검사를 하면 기존의 ELISA로 발견하지 못하였던 과거 감염의 증거를 찾을 수 있습니다. CagA 항체가 다른 항체에 비하여 오래 지속되기 때문입니다.
FAP 환자에서도 간혹 위 종양이 발생합니다.
Nakamura K. Endoscopy International Open 2017
Pyloric gland adenoma는 misnomer입니다 (Hashimoto. Histopathology 2015). 왜냐하면 이름과 달리 fundic gland에서 발생하기 때문입니다. Background gastric mucosa는 atrophic한 경우가 많은데 특히 autoimmune atrophy와 관련이 있습니다 (Vieth M. Virchows Arch 2003).
EBV positive gastric cancer (Gastroenterology 2009;137:824-33, Fukayamo M. Pathology International 2010:60:337-50, Wu Gastroenterology 2000;118:1031-8). 남자에 많고 lymphoepithelioma-like lesion이 있습니다. 대부분 Hp 감염이 있습니다. EBV가 Hp 없이 단독으로 위암을 일으키는 경우는 매우 적습니다. EBV-related Hp negative gastric cancer is very rare (Gastroenterology 2015;129:2058-63).
Pernicious anemia가 autoimmune gastritis와 같은 말은 아닙니다. Autoimmune gastritis의 일부는 Hp 감염과 관련되어 있습니다. Hp감염자에서 parietal cell에 대한 자가 항체가 흔히 발견됩니다 (Helicobacter 2001;6:225-33). Hp negative autoimmune gastritis에서 (type I carcinoid가 종종 발생하지만) 위암 발생은 rare 합니다 (Rugge. APT 2012:35:1460). Pyloric gland adenoma의 일부는 autoimmune gastritis와 관련이 있습니다 (Virchows Arch 2003;442:317-21).
Hp negative gastric cancer에서도 differentiated type이 undifferentiated type 보다 많았습니다. 특이한 점은 gastric cancer with fundic gland differentiation을 보이는 경우가 많다는 것입니다.
GC occurring after eradication of H. pylori는 국가에 따라 다른 양상을 보입니다. 일본에서는 대부분 조기위암이었고 overseas에서는 진행성 위암이 많았습니다. 아마도 missed cancer였을 가능성이 큽니다. 제균치료 후 발생하는 위암의 위험인자는 역시 위축성 위염입니다.
Sugano 교수님의 멋진 강의는 아래와 같은 슬라이드로 끝났습니다.
 2. 2017년 8월 27일 내시경학회 세미나 송경호 교수님 강의
2. 2017년 8월 27일 내시경학회 세미나 송경호 교수님 강의
아주 차분하고 멋진 강의였습니다. 내시경 세미나라는 큰 무대에 멋지게 데뷔하신 것 축하합니다. 강의 원고도 좋았습니다. 옮깁니다.
1) 서론
헬리코박터 파일로리가 위암의 주요 원인인 것은 주지의 사실이다. 특히 두 개의 전향적 코호트 연구들은 헬리코박터 파일로리 감염자에 한해서만 위암이 발생한다고 결론지었다. 이후로 실제 임상에서는 헬리코박터의 감염 증거가 없는 정상 위 점막 배경에서도 위 선암을 진단한 예들을 경험하게 되었다. 이에 일본, 한국, 대만 등에서 헬리코박터 음성 위암(Helicobacer pylori-negative gastric cancer, HPNGC)에 대한 역학 및 병리학 연구들이 나오고 있다. 헬리코박터 제균 치료, 보다 나은 위생을 통해 헬리코박터 감염 유병률은 꾸준히 감소하고 있다. 2015년 혈청 검사를 통한 우리나라 헬리코박터 감염률은 51.0%이며, 1998년의 66.9%에 비해 지속적으로 감소되었음을 확인하였다. 헬리코박터 감염률의 지속적인 저하에 따라 HPNGC에 대한 관심은 상대적으로 증가할 수 있다. HPNGC에 대한 연구는 헬리코박터 균 이외에 새로운 위암 원인을 확인하게 도와 줄 수 있다. HPNGC에 대한 연구는 소화기내시경 검진의사에게 헬리코박터 감염의 증거가 없는 정상 위 점막을 검진하면서도 유의해서 관찰해야 부위와 일부 특징적인 모양의 위암의 발견을 위한 노력을 기울이게 도와준다. 임상에서 헬리코박터 음성의 경우는 세 가지로 분류할 수 있다: 1) 헬리코박터 검사의 위음성, 2) 헬리코박터 감염 후 제균 상태, 3) 헬리코박터 비감염 상태 이다. 본 강의에서는 헬리코박터 비감염자(Helicobacter pylori-naive state)에서 발생하는 위암을 주제로 HPNGC의 역학, 임상양상, 일부 특징적인 내시경 진단을 헬리코박터 양성 위암과 비교하여 소개하였다.
2)본론
2-1) HNPGC의 정의
헬리코박터의 현성 감염 및 과거 감염이 없는 상태를 선별하기 위한 진단기준은 많은 난점이 있다. 이는 헬리코박터 감염이 진행됨에 따라 위 점막의 위축과 장상피화생이 발생하고 이로 인해 헬리코박터 균의 진단율이 급격하게 저하되는 low bacterial load의 상태로 변화되기 때문이다. 또한 경도의 위 점막의 위축을 내시경과 생검으로 진단하는 데에는 한계가 있다. 위 점막의 위축은 헬리코박터 감염의 유병률이 높은 지역에서는 대부분 헬리코박터 감염에 의한 것이므로, 위 점막의 위축 여부를 판단하는 것은 헬리코박터 감염력이 없는 상태 (Helicobacter pylori-naive state)를 진단하는 데 있어 중요한 축이다. Yamamoto 등은 HPNGC의 진단 기준을 제시하여 내시경, 생검 조직, 혈청 Pepsinogen assay 중 두 가지 이상이 위 점막 위축이 없는 상태이면서 요소호기 검사나 혈청 anti-Helicobacter pylori IgG가 음성인 위암 환자로 정의할 것을 권고하였다.
(1) 내시경 진단
헬리코박터 감염력이 없는 상태의 위 점막은 백색광 내시경 관찰 시 점막의 집합세정맥(collecting venule)이 위 전체에 유지되어 있다. 5 병리학적으로 위 점막 표면에는 위 소구들(gastric pits)이 점의 형태로 보이며, 위 소구 주변에 미세혈관과 이들이 모여서 보다 굵은 집합세정맥들이 분포한다. 확대내시경이 아닌 일반적인 백색광 내시경으로는 위 소구와 미세혈관을 관찰할 수 없으나 집합세정맥은 불가사리 모양과 흡사한 형태로 관찰이 가능하다. 위 점막의 집합세정맥을 관찰하는데 있어 주의해야 할 것은 관찰 부위의 선정이다. 십이지장 궤양, 젊은 헬리코박터 감염자의 경우 위 상체부나 중체부까지 집합세정맥의 정상적은 분포가 유지될 수 있다. 이에 반해, 하체부 소만을 진단의 근거로 삼았을 경우에는 규칙적인 집합세정맥의 분포가 유지되는 경우 감염자가 하나도 없었고, 집합세정맥의 분포가 없어진 경우의 87%에서 헬리코박터 감염을 확인하였다. 이를 근거로 하체부 소만의 규칙적인 집합세정맥의 분포의 관찰은 헬리코박터 감염력이 없는 상태의 진단에 유용하다. 접합세정맥의 분포 외에도 위 전정부의 선상의 발적, fundic gland polyp이 위 감염력이 없는 상태와 연관성이 있다.
자가면역성 위염과 달리 헬리코박터 감염에 의한 위 점막의 위축은 전정부로부터 시작되는 특징이 있다. Kimura-Takemoto 분류에 따라 위축의 정도를 판정하는 것이 일반적이며 정상 점막과 위축된 점막의 경계부위를 관찰하는 것이 중요하다. 왜냐하면 내시경 검사 중 송기량이 과할수록 위 저부의 점막하 혈관상이 뚜렷해 질 수 있기 때문이다. 이런 경우에 위 저부 점막의 위축으로 혼동할 여지가 있다. HPNGC 관련 연구들에서는 위점막의 위축이 없거나 Kimura-Takemoto classification C-I까지를 헬리코박터 감염력이 없는 상태의 가능한 위 점막의 상태로 분류하였다.
(2) 생검 조직 진단
업데이트된 Sydney system에 준하여 표준화된 다섯 군데(체부 두 군데, 각부, 전정부 두 군데)의 위 점막 조직을 분석하여 헬리코박터의 현성 감염이나 과거 감염을 추정한다. 7 Sydney system의 기준으로 위 선의 위축 (0점), 장상피화생 (0 또는 1점), 단핵구 침윤 (0또는 1점), 중성구 침윤 (0점), H. pylori 밀도 (0점)인 경우에 점막의 위축이 없고, 헬리코박터의 감염력이 없는 것으로 판단할 수 있다.
(3) Pepsinogen assay 위 선의 chief cell, mucus neck cell은 pepsinogen을 생성한다. 위 점막의 위축이 광범위해질수록 혈청의 pepsinogen의 양상은 변화한다. Pepsinogen I은 위 저부에서만 생성되는 반면, Pepsinogen II는 전체 위 조직과 십이지장 구부에서 생성된다. 위 점막의 위축이 없는 경우에는 혈청 Pepsinogen I >70ng/mL, Pepsinogen I/II ratio >3.0으로 유지되고 위 점막의 위축이 저부까지 광범위해지면 Pepsinogen I의 저하가 두드러지면서 Pepsinogen I의 저하 및 Pepsinogen I/II ratio의 저하가 심화된다. 이러한 Pepsinogen assay의 결과 위 점막의 위축이 없는 것으로 나올 경우 음성예측도 99%이상으로 정상 위 점막으로 진단할 수 있다. 반면 헬리코박터 감염자가 제균 치료를 받은 뒤 12개월이상 경과 시에는 상당 부분 감염력이 없는 정상인의 수치와 차이가 없어지면서 정상화 되기도 한다. 그러므로, 혈청 Pepsinogen의 해석을 할 경우에는 제균 치료력을 고려해서 위 점막의 위축을 판단해야 한다.
2-2) 역학 연구
Kato 등은 일본인 위암 환자 748명을 대상으로 혈청 헬리코박터 항체와 Pepsinogen assay을 통해서 HPNGC의 비율을 계산하였다. 대상자의 14.2%에서 혈청 항체가 음성이었고 2.0%의 환자가 Pepsinogen assay 위축 음성이었다. 대상자의 3.6%는 혈청 헬리코박터 항체 음성이면서 동시에 광범위한 위 점막 위축 양성이었다(Pepsinogen I <30ng/mL, Pepsinogen I/II ratio <2.0). 그러므로 3.6%의 혈청 음성 환자는 심한 위축성 위염으로 인한 헬리코박터 균의 자연 소실과 항체 정상화로 분류할 수 있었다. 이를 근거로 해당 병원의 HPNGC의 비율은 최소 2.0%, 최대 10.6%(14.2% 빼기 3.6%)로 산정하였다. Matsuo 등은 일본인 위암 환자 3161명을 대상으로 혈청 헬리코박터 항체, 생검 결과, 내시경 진단, 요소호기검사, RUT 등을 순차적으로 시행하여 최종적으로 0.66%의 낮은 비율을 확인하였다. 매우 엄격한 HPNGC의 기준(내시경 진단, 생검 진단, Pepsinogen assay, 혈청 헬리코박터 항체, 요소호기검사, RUT, 대변 항체, 제균 치료력을 모두 고려)을 적용한 두 개의 일본 역학 연구의 결과로는 각각 0.42%와 2.3%의 비율을 확인하였다. 윤 등은 한국인 위암 환자 627명을 분석하여 5.4%의 비교적 높은 HPNGC의 비율을 보고하였다. 이는 일본의 보고들에 비해 비교적 높은 비율이다. 높은 HPNGC의 이유 중 하나로 Pepsinogen assay를 통해서 광범위한 위축성 위염 환자들만을 배제하고 경도 및 중등도 위축성 위염 환자들은 포함한 기준이 있다. 헬리코박터 감염 유병률이 낮은 나라들의 HPNGC의 비율은 13.8%~24.6%로 비교적 높음을 알 수 있다.
이상을 정리하면, 헬리코박터 감염률이 높은 나라에서는 1% 안팎, 감염률이 낮은 나라에서는 20% 안팎의 HPNGC의 유병률을 확인할 수 있다.
2-3) 임상적 특징
HPNGC의 정의가 연구마다 상이하고, 케이스 수도 많지 않은 단일 기관 분석의 한계로 인해 HPNGC의 일반적인 임상적인 특징을 기술하기는 어렵다. 보고된 연구들의 많은 수에서 60세 미만의 비교적 젊은 연령이라는 점, 남녀 성비가 0.7~2.5 정도로 비교적 여성 환자가 많은 점, 미분화형 암의 비율이 42.9~100%로 높은 점은 주지할 만하다. 근위부 암의 비율은 25% 정도로서, 헬리코박터 양성인 위암에 비해 13% 가량 높다.
내시경 진단의 특징은 Chief cell predominant type의 위암의 경우 비교적 특징적이다. 점막하종양의 형태, 황백 색조, 병변 내 모세혈관상의 두드러진 혈관의 모양 등 비교적 특별한 모양을 띈 경우가 많다(후술). HPNGC가 헬리코박터 양성 위암에 비해 예후가 나쁘다는 보고들이 있다. Stage II이하, Stage III이하, 모든 병기에서 HPNGC의 예후가 헬리코박터 양성 위암에 비해 나빴다. 이러한 경향은 다른 나쁜 예후인자들을 보정하고서도 유지되어, Helicobacter pylori-naive state 자체가 위암의 독립적인 나쁜 예후인자로 보고하였다. 암 전이와 관계 있는 E-Cadherin, microsatellite instability, matrix metalloproteinase 등이 이러한 나쁜 예후와 연관이 있을 것으로 추정하고 있다. 반면 Chief cell predominant type의 위암은 치료 없이 평균 58개월 이상 경과 관찰한 11예(이중 HPNGC는 3예) 모두에서 진행이 없었다. 진행성 위암으로 진단된 fundic gland type의 위암은 증례 보고 수준이다.
2-4) HPNGC의 다양한 형태들
(1) Lymphoepithelioma-like carcinoma
Epstein-Barr virus 감염은 비인두 림프상피종과 유사한 형태의 위암을 유발할 수 있다(lymphoepithelioma-like carcinoma, LELC). 24 대부분의 EBV 양성 위암은 위축성 위염과 동반된 상태이나 헬리코박터 감염율은 비교적 낮다. 위 근위부의 미분화형 선암의 형태로 진단되는 특징이 있다. 우리나라의 연구에서도 이러한 경향은 유지되었고, LELC는 독립적인 예후인자는 아니었다.
(2) Germline mutation (CDH1 gene mutation)
Diffuse-type gastric cancer의 주요 병인 중 하나인 CDH1 유전자 변이는 상피세포 유착 물질인 E-Cadherin을 코딩 하는데 이상이 있다. 28 유전적 미만형 위암의 환자들에게서도 CDH1 유전자의 germline mutation을 확인할 수 있다. Germline CDH1 mutation이 있는 환자들은 일생에 위암이 생길 위험이 70%이상, 유방암이 생길 위험이 40%이상이다. 유전적 미만형 위암의 경우 미분화형 위암이 다발성으로 생길 위험이 높으므로 예방적 위 전절제술을 권고한다. 2010년 International Gastric Cancer Linkage Consortium은 가족력이 없는 40세 미만의 미만형 위암 환자는 CDH1 유전자 변이 검사를 받을 것을 권고하였다.
(3) Chief cell predominant type
위 점막의 oxyntic mucosa에서 기원하는 분화도가 좋은 일부 위암은 조직학적으로 fundic gland와 유사하여, Gastric adenocarcinoma of the fundic gland type-Chief cell predominant type (GA-FG-CCP) 으로 불린다. 이 종양은 mucous neck cell이 chief cell로 분화하는 저위도 비정형 세포의 형태이다. 비교적 점막의 기저부에서 발생하므로, 점막하 종양의 형태를 띄면서 점막은 정상 상피인 경우가 흔하다. 점막하 종양의 형태일 경우 위 신경내분비종양과 감별을 요한다. 편평하거나 함몰형의 경우 국소적인 위축, 미만성 위암, 위 말트종과 감별을 요한다. 이 십 예의 GA-FG-CCP를 분석한 일본 보고에서는 모든 예가 위 체부의 병소이며, 대부분 1cm 미만의 작은 크기이었다. 절제 예의 80%에서 점막하 침윤이 존재하였으나 림프관 침윤은 없었다. 또한 종양의 Ki-67 index도 낮았다. 평균 58개월이상 경과 관찰한 모든 예에서 암의 진행은 없었다.
3.요약
제균 치료 등으로 헬리코박터 감염 유병률은 지속적으로 감소하고 있고, 상대적으로 HPNGC에 대한 관심은 증가할 수 있다. 헬리코박터 감염력이 없는 상태를 진단하기 위해서는 위 점막의 위축 정도를 파악하는 것이 중요하며, 하체부 소만의 집합세정맥의 분포, 혈청 Pepsinogen assay 등을 통해 객관적으로 판단할 수 있다. 우리나라와 일본에서 HPNGC의 비율은 전체 위암의 1~5%가량이며, 서구에서는 이보다 훨씬 높다. HPNGC는 헬리코박터 양성 위암에 비해 미분화형과 위 근위부암의 비율이 높다. GA-FG-CCP등 특징적인 내시경 형태를 숙지하여 그 진단율을 높일 수 있으며, 유전적 미만형 위암 환자에게 유전자 변이 검사를 고려해야 한다.
Helicobacter negative gastric cancer는 일본에서 꼼꼼히 연구되는 분야입니다. Digest Endosc 2015년 7월호에 관련 리뷰가 실렸습니다 (Yamamoto Y. Digest Endosc 2015).
Helicobacter pylori (H.pylori) leads to chronic gastritis and eventually causes gastric cancer. The prevalence of H. pylori infection is gradually decreasing with improvement of living conditions and eradication therapy. However, some reports have described cases of H. pylori-negative gastric cancers (HpNGC), and the prevalence was 0.42-5.4% of all gastric cancers. Diagnostic criteria of HpNGC vary among the different reports; thus, they have not yet been definitively established. We recommend negative findings in two or more methods that include endoscopic or pathological findings or serum pepsinogen test, and negative urease breath test or serum immunoglobulin G test and no eradication history the minimum criteria for diagnosis of HpNGC. The etiology of gastric cancers, excluding H. pylori infection, is known to be associated with several factors including lifestyle, viral infection, autoimmune disorder and germline mutations, but the main causal factor of HpNGC is still unclear. Regarding the characteristics of HpNGC, the undifferentiated type (UD-type) is more frequent than the differentiated type (D-type). The UD-type is mainly signet ring-cell carcinoma that presents as a discolored lesion in the lower or middle part of the stomach in relatively young patients. The gross type is flat or depressed. The D-type is mainly gastric adenocarcinoma of the fundic gland type that presents as a submucosal tumor-like or flat or depressed lesion in the middle and upper part of the stomach in relatively older patients. Early detection of HpNGC enables minimally invasive treatment which preserves the patient's quality of life. Endoscopists should fully understand the characteristics and endoscopic findings of HpNGC.
(1) 비교적 젊은 나이의 signet ring cell carcinoma와 (2) proximal stomach의 flat 혹은 SMT-like한 fundic gland type cancer가 특징적인 소견이라고 합니다. 리뷰의 사진을 옮깁니다.
Undifferentiated-type early gastric cancer (GC). The patient was a 36-year-old man. He had no symptoms and was detected with early GC by screening endoscopy. (a,b) There was no Helicobacter pylori infection in the stomach. (c) The lesion is slightly discolored, depressed and located at the upper body greater curvature (yellow arrows). Lesion size is 11 mm. (d) He underwent endoscopic submucosal dissection, and pathological findings revealed signet ring-cell carcinoma that was limited to the mucosal layer.
Gastric cancer (GC) of fundic gland type. The patient was a 62-year-old man. He had no symptoms and was detected with early GC by screening endoscopy. (a,b) There was no Helicobacter pylori infection in the stomach. (c) The lesion is whitish, slightly depressed and located in the gastric cardia posterior wall. Dilated vessels are seen on the surface of the lesion (yellow arrows). Lesion size is 10 mm. (d) He underwent endoscopic submucosal dissection, and pathological findings revealed adenocarcinoma of the fundic gland type that was limited to the mucosal layer.
 4. 이선영 교수님의 2020년 리뷰와 2021년 강의
4. 이선영 교수님의 2020년 리뷰와 2021년 강의
[2017-8-29. 애독자 질문]
헬리코박터 음성 위암에 대한 글 (2017 내시경학회세미나 송경호 교수님 강의록) 잘 읽었습니다. 증례는 많지 않지만 제가 경험한 (1) Lymphoepithelioma-like carcinoma와 (2) CDH1 gene mutation은 흥미롭게도 대부분이 Hp 양성으로 보고되어서 문헌들을 찾아본 적이 있었는데, 일본인 위암환자의 CDH1 gene mutation 상당수는 Hp 감염으로 인한 손상으로 나타나며, 서양과 달리 일반적인 장형위암처럼 좋은 경과를 보인다는 문헌이 있었습니다.
제로 제가 경험한 CDH1 gene mutation을 보인 AGC 환자들 중에도 수술 후 10년 가까이 재발없이 잘 지내고 계신 분들이 있습니다. 그래서인지 우리나라에서는 "CDH1 gene mutation을 보인 위암 환자 = Hp음성 = 서양처럼 예후가 매우 나쁘다"라고 강의가 되는 경우가 많습니다. 어떻게 생각하시는지요?
[2017-8-30. 송경호 교수님 답변]
저도 경험이 많지 않아 좋은 답변을 드릴만한 위치는 아닌 것 같습니다. HPNGC (Helicobacter negative gastric cancer)에 대한 역학 자료를 볼 때 'Hp 양성 위암에 비해 Hp 양성율이 낮다'로 보는 게 맞다고 생각합니다. Fundic gland type GC에서도 Hp 양성률이 40-50% 정도 되는 것처럼 다른 형태의 암에서도 Hp 감염은 by-stander, 또는 병인에 일부라도 관여하지 않을까 추측합니다.
Lymphoepithelioma-like carcinoma에 Hp 병인은 아직은 확실치 않은 것으로 생각합니다. 어떠한 연구에서는 Hp감염과 연관성이 없고, 어떠한 연구는 Hp감염과 연관성이 있었습니다. 다만 많은 증례에서 위점막위축과 연관이 있다는 점인데요. 이를 보면 EBV 단독으로 또는 Hp 감염과 함께 복합적인 프로세스로 발암이 되었다고 생각합니다.
CDH1 gene mutation에 대한 예후는 제 강의에서는 다루진 않았습다만, 이것이 확인된 환자들은 본인과 주변 가족들에게 annual surveillance exam을 강조하거나, Diffuse type GC가 확인되었다면 total gastrectomy를 고려해야함을 강조하였습니다.
[2017-9-3. 한 애독자 편지]
송경호 선생님의 귀한 답변 잘 읽었습니다. 한국인에서는 순수한 HPNGC or lymphoepithelioma-like carcinoma는 드물거라는 의견에는 동의합니다. 다만 CDH1 gene mutation 환자 본인과 주변 가족들에게 annual surveillance exam을 강조하거나, Diffuse type GC가 확인되었다면 total gastrectomy를 고려해야 한다는 의견에는 반대합니다. 왜냐하면 한국인 위암 환자들은 Hp 감염으로 인한 CDH1 hypermethylation이 흔해서, 서양에서 발견되는 CDH1 gene mutation 자체로 인한 순수한 familial diffuse-type GC와 본질적으로 다르기 때문입니다.
현재 국내대학병원에서는 위암수술 후에 CDH1 변이 여부를 e-cadherin 면역염색 결과로 판단하여 제시하고 있기 때문에, CDH1 변이가 있다고 나와도 굳이 주변 가족들에게 이 때문에 annual surveillance exam을 강조할 필요는 없으며, 설사 diffuse type GC가 확인되었더라도 이 때문에 total gastrectomy를 권할 필요는 없다는 것이 제 생각입니다.
[2021-9-3. InterMD 내시경 세미나 질문]
이선영 교수님의 2020년 리뷰를 잘 보았습니다. Helicobacter 음성 signet ring cell carcinoma는 '유문선와 위저선의 경계선'에서 발생한다고 되어 있는데 구체적인 위치는 어디입니까?
[2021-9-3. 이준행 답변]
아래 그림을 참고하시기 바랍니다. 유문선과 위저선의 경계는 위체하부와 근위전정부 사이 정도입니다.
2) [Review] Hp 음성 위암 (이선영 2020)
3) 자가면역성 만성 위축성 위염과 연관하여 발생한 위 신경내분비종양 Neuroendocrine tumor associated with autoimmune gastritis (대한소화기내시경학회 2021-8 교육자료)
 © 일원내시경교실 바른내시경연구소 이준행. EndoTODAY Endoscopy Learning Center. Lee Jun Haeng. (since 1999-8-23)
© 일원내시경교실 바른내시경연구소 이준행. EndoTODAY Endoscopy Learning Center. Lee Jun Haeng. (since 1999-8-23)