 EndoTODAY 내시경 교실
EndoTODAY 내시경 교실
Beginner | ESA | Schedule | OPD
Seminars | Atlas | Recent | Links
 [Signet ring cell carcinoma (SRC). 반지세포암. 인환세포암] - 終
[Signet ring cell carcinoma (SRC). 반지세포암. 인환세포암] - 終
1. Definition of signet ring cell carcinoma
2. ESD for undifferentiated type EGC at Yonsei University
3. Growth pattern of signet ring cell carcinoma
4. SRC 확대내시경 소견 - stretch sign
5. Cases
6. FAQs - 2014년 대토론, signet ring cell change와 조직검사 false positive
7. References
반지세포암은 암 덩어리가 반지처럼 생긴 것이 아니라 암 세포가 반지 모양이라는 뜻입니다.
 1. Definition of SRC (signet ring cell carcinoma)
1. Definition of SRC (signet ring cell carcinoma)
Signet-ring cell carcinoma (SRC) is defined as a tumor that predominantly consists of isolated or small groups of tumor cells containing intracytoplasmic mucin.
넓은 의미의 poorly cohesive carcinoma는 4개의 cell type이 있습니다. 이를 WHO 2010에서는 둘로 나누고 있습니다.
| 4 cell types of poorly cohesive carcinoma | WHO 2010 |
| 1. Nuclei push against cell membranes by intracytoplasmic mucin (typical SRC) | Poorly cohesive carcinoma, SRC phenotype |
| 2. Central nuclei with intracytoplasmic mucin | Poorly cohesive carcinoma, other cell types (일본의 Por2 (non-solid type)에 해당) |
| 3. Eosinophlic cytoplasmic mucin | |
| 4. Cells without mucin |
일본에서는 poorly cohesive carcinoma 중 SRC type을 SRC로 부릅니다. 나머지 cell type은 Por2 (non-solid type)라고 부릅니다. 전통적인 의미의 poorly differentiated tubular adenocarcinoma는 WHO 2010에서는 Poorly differentiated tubular (solid) carcinoma라고 부릅니다.
Poorly라고 시작하는 종류는 아래 표와 같이 세 개입니다. 셋을 둘로 나누는 방법이 상당히 헷갈립니다. WHO 2010에서는 poorly cohesive carcinoma라는 이름으로 두 group(노란색)을 묶었고, 일본에서는 Por라는 이름으로 두 group(연두색)을 묶었습니다. 즉 일본에서는 SRC을 별개의 질환으로 하고 Por1과 Por2를 비슷하다고 본 것 같습니다.
| WHO 2010 | Japanese 2017 | 이준행의 해석 | |
| Poorly differentiated (solid) carcinoma | Por1 (solid type) | 전통적인 P/D | 미만형보다 장형에 가깝다. |
| Poorly cohesive carcinoma, SRC phenotype | Signet ring cell carcinoma | Poorly cohesive 中 cell type 1 | |
| Poorly cohesive carcinoma, other cell types | Por2 (non-solid type) | Poorly cohesive 中 cell type 2, 3, 4 | 미만형 |
* 참고: 제57회 내시경 세미나 주미 교수님 강의
* 참고: Consensus on the pathological definition and classification of poorly cohesive gastric carcinoma Gastric Cancer 2019
A consensus was reached on the need to classify gastric carcinoma according to the most recent edition of the WHOclassification which is currently WHO 2010. Moreover, to standardize the definition of SRC carcinomas, the proposal that only WHO PC carcinomas with more than 90% poorly cohesive cells having signet ring cell morphology have to be classified as SRC carcinomas was made. All other PC non-SRC types have to be further subdivided into PC carcinomas with SRC component (<90% but >10% SRCs) and PC carcinomas not otherwise specified (<10% SRCs).
즉 다음과 같이 나누었다는 의미입니다.
- Signet ring cell이 90%를 초과하면: signet ring cell carcinoma
- Signet ring cell이 10-90%면: poorly cohesive carcinoma with signer ring cell component
- Sigent ring cell이 10% 미만이면: PCC-NOS
[Advances in surgical pathology. Gastric cancer (2011)]
Signet ring cell and other poorly cohesive carcinomas (60쪽)
SRCCs are tumors composed solely of signet ring cells. However, many tumors are composed of a mixture of poorly cohesive non-signet ring cells as well as signet ring cells. In many cases, signet ring cells are restriced to the upper half of the a mucosal component of the tumors in combination with poorly cohesive cells withing deeper levels of the gastric wall. Poorly cohesive non-signet ring cells include those that resemble plasma cells, histiocytes, or lymphocytes. The tumor cells of poorly cohesive carcinomas can be arranged in lace-like gland or delicate microtrabecular patterns. Usually, they are accompanied by marked desmoplasia in the gastric wall.
[Blue book - WHO classification (2019)에 언급된 PCC, SRC]
Poorly cohesive carcinoma (PCC), including signet-ring cell carcinoma and other subtypes
PCCs account for 20-54% of GCs, with higher frequencies reposrted in Japanese patients. PCCs are composed of neoplastic cells that are isolated or arranged in small aggregates without well-formed glands. PCCs can be of either signet-ring cell type of non-signet ring cell type (PCC-NOS). Signet-ring cell type tumors are composed predominantly or exclusively of clear, globoid droplet of cytoplasmic mucin with an eccentrically placed nucleus. Singet-ring cells may form a lace-like glandular or delicate microtrabecular pattern (especially in the mucosa). Other cellular subtypes (non-signet-ring cell type: PCC-NOS) include tumors composed of neoplastic cells resembling histiocytes or lymphocytes: others have deeply eosinophilic cytoplasm; some poorly cohesive cells are pleomorphic, with bizarre nuclei. A mixture of the different cell types can be seen, including few signet-ring cells. PCCs can be accompanied by marked desmoplasia, in particular when infiltrating into the submucosa or beyond.
정상 gland 옆에서 Paget 양상으로 자라다가 점차 gland 사이의 lamina propria를 차지하고 점차 gland와 gland 사이의 간격을 넓히는 stretch sign으로 발전하고 이후 더 커져서 mass가 됩니다.
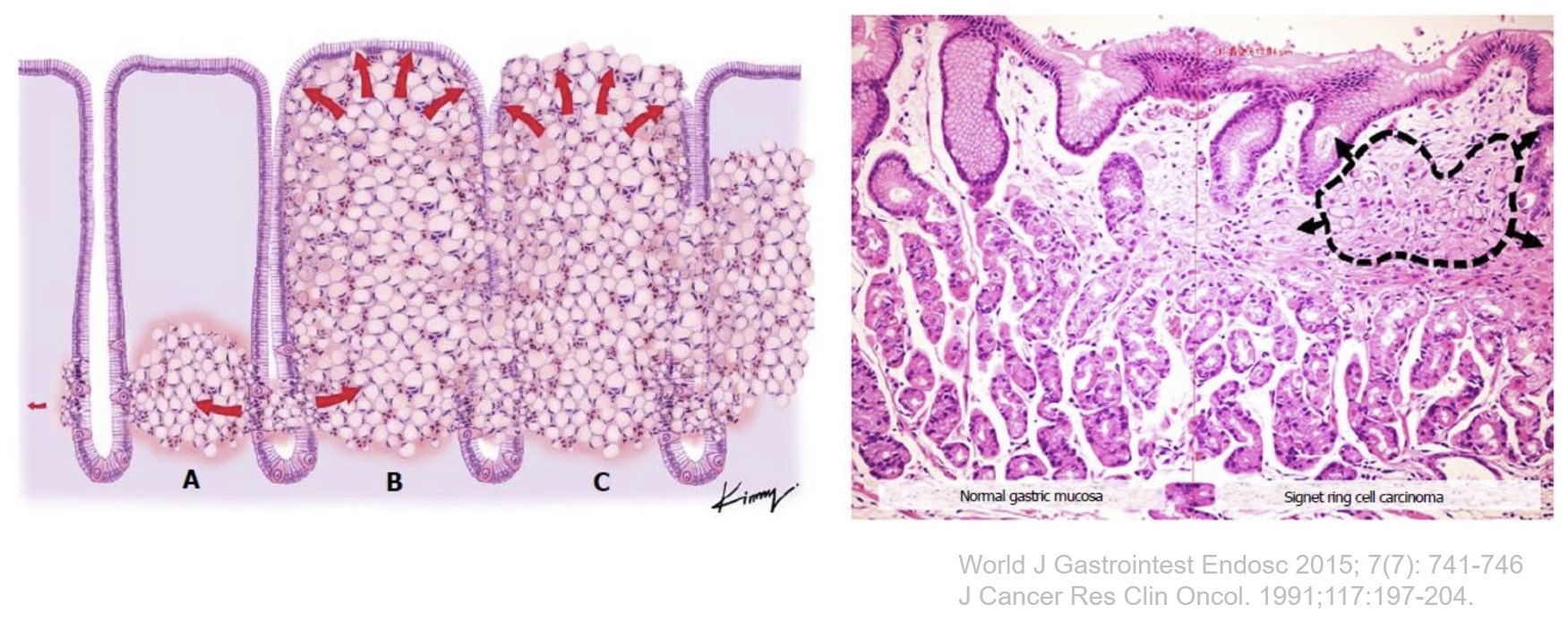
Figure 3 Theoretical view of the pathophysiology of signet ring cell differentiation: (A) tumor cells originating in the neck of the gland and spreading to the submucosal space; (B) an increasing number of tumor cells being packed together, resulting in a barrel shape; and (C) the previously non-exposed tumor becoming exposed through necrosis and formation of an ulcer.
Figure 4 Microscopic view of a signet ring cell gastric carcinoma, demonstrating: (1) normal appearing gastric mucosa (left); and (2) signet ring cells (black dashed circle) causing distortion of the gastric glands (right), consistent with the endoscopic finding of the “stretch sign. ”
 2. ESD for undifferentiated type EGC at Yonsei University
2. ESD for undifferentiated type EGC at Yonsei University
Gut and Liver 2015년 11월호에 실린 연세대학교 김지현 교수님 등의 Growth patterns of SRC for endoscopic resection (Kim H. Gut Liver 2015) 논문을 흥미롭게 보았습니다.
연세대학교에서는 오래 전부터 undifferentiated type EGC의 내시경치료 성적을 꾸준히 발표하였습니다. 첫 중요 성과는 2009년 GIE에 발표한 아래 자료였습니다 (Kim JH. GIE 2009). Poorly differentiated adenocarcinoma에서는 vertical margin 양성이 많고, signet ring cell carcinoma (SRC)에서는 lateral margin 양성이 많았습니다.
2014년 연세대학교 강남병원에서는 undifferentiated type EGC 내시경치료 장기성적을 발표하였습니다 (Kim JH. GIE 2014).
2014년 연세대학교 신촌병원에서는 SRC에 대한 내시경치료를 따로 분석하여 발표하였습니다 (Kim MN. DLD 2014). 예상되었던 바와 같이 Size underestimation된 경우(=작다고 생각하여 ESD 하였는데 실제로는 작지 않은 예)에서 incomplete resection이 많았습니다.
아주 작은 signet ring cell carcinoma는 내시경으로 치료할 수 있습니다. 큰 것은 조심해야 하겠지요.
 3. Growth pattern of signet ring cell carcinoma
3. Growth pattern of signet ring cell carcinoma
SRC는 내시경으로 크기 및 경계 판정이 어렵고, 결국 ESD에서 lateral margin 양성으로 나타난다고 해석됩니다. 이번에 김지현 교수팀은 SRC를 병리학적 growth pattern을 바탕으로 expanding type과 infiltrative type으로 나누어 분석하였습니다 (Kim H. Gut Liver 2015).
The expanding type was defined as a tumor that had a margin that was clearly lined from the non-neoplastic mucosa, that is, epithelial spreading pattern.
The infiltrative type was defined as a tumor that showed diffuse spreading tumor cells, that is, supepitheial spreading pattern.
Signet ring cell carcinoma intramucosal spreading types. Expansive type. (A) Tumor cells (circle) were exposed at a superficial part of the mucosa. A tumor with a margin was distinct from the nonneoplastic mucosa (H&E stain, ×40). (B) Tumor cells (circles) were located in the intermediate or deeper parts of the nonneoplastic mucosa. Diffuse-spreading tumor cells were evident (H&E stain, ×40).
대략 expanding type과 infiltrative type이 반반이었는데, infiltrative type의 주변 점막에 atrophy와 intestinal metaplasia가 많았습니다. 저자는 surrounding mucosa가 SRC의 tumor cell spread의 mechanical barrier일 수 있다고 해석하였습니다. 무척 흥미롭습니다.
This indicates that the surrounding mucosa may be important as a mechanical barrier to tumor cell spread in SRC. If mechanical barrier represented by the surrounding mucosa is weak, such as due to atrophy/IM or no neutrophil infiltration, tumor cells tend to spread spontaneously or diffusely into the deeper part of the mucosa.
저자는 SRC의 내시경 경계판정이 어려운 이유로 SRC의 기원이 여느 위선암과 다르다는 점을 지적하면서 tubule neck dysplasia (TND)가 SRC의 precursor라는 병리 논문(Kumarasinghe MP. Pathology 2006)을 인용하였습니다 (아쉽게도 논문 PDF를 구할 수 없었습니다).
Tubule neck dysplasia can spread upwards towards the foveolar surface and possibly downwards to the gastric glands. The gastric mucosa of SRC may show a largely intact surface epithelium, despite the presence of cancer in the lamina propria.
김지현 교수님 논문에 대하여 부산대학교 김광하 교수님께서 논평을 붙이셨습니다 (Kim GH. Gut Liver 2015). 색소내시경이나 확대내시경이 undifferentiated type 위암의 경계판정에 도움을 주지 못하는 현실(Lee BE. BMC Gastroenterology 2010)에서 김지현 교수님의 의견이 중요하다고 지적하셨습니다.
Several studies have shown the efficacy of acetic acid-indigo carmine chromoendoscopy and magnifying endoscopy with narrow-band imaging to identify the horizontal margins of differentiated-type carcinoma.However, these techniques do not give additional information to delineate the horizontal margins of undifferentiated-type carcinoma, especially SRC, because of the subepithelial spreading tendency of SRC.
아래는 김광하 교수님의 2010년 논문(Lee BE. BMC Gastroenterology 2010)에 나온 사진입니다. Undifferentiated type에서는 색소내시경도 별 볼일이 없다는 결론이었습니다.
Chromoendoscopy of an undifferentiated adenocarcinoma. (A) A flat discolored lesion with an unclear border at the lower body of the stomach is shown. (B) Endoscopic view after acetic acid was sprinkled. (C) Endoscopic view after indigo carmine was additionally sprinkled. (D) Endoscopic view after the lesion was washed with clean water. After chromoendoscopy with indigo carmine dye added to acetic acid, the lesion's border was still indistinct and the image was mottled. The lesion was resected by laparoscopic gastrectomy and was shown to be an undifferentiated adenocarcinoma.
조기위암 내시경치료를 전문하는 의사의 입장에서 김지현 교수님 논문에 제시된 아래 사진이 무척 교훈적으로 다가왔습니다. 작은 SRC로 생각하여 ESD 하였으나 여러 방향의 multiple lateral margin 양성이 나온 경우였습니다. 작은 SRC로 추정되더라도 주변 점막이 atrophic하면 infiltrative type growth (= subepithelial spreading pattern)의 가능성을 고려하여 더욱 주의해야 할 모양입니다.
Clinical case of the infiltrative intramucosal-spreading type of signet ring cell carcinoma (SRC). (A) Endoscopic image of early gastric cancer showing a flat lesion located in the lesser curvature of the lower body (circle). Endoscopically, the surrounding mucosa was combined with atrophic gastritis. (B) After endoscopic resection, three lateral margins were positive (circles). (C) Pathological findings after endoscopic resection (H&E stain, ×40). SRC cells exhibited subepithelial spread, indicating that the lesion was of the infiltrative type (circle).
사실 저는 undifferentiated type 조기위암의 내시경 치료는 극히 드물게 시행하고 있을 뿐입니다. 논문을 낸 적이 있지만 몇 예 되지 않았습니다 (Dig Dis Sci 2014). 향후 좀 시행할까 싶어서 기초 자료를 분석하여 2015년 소화기학회에서 발표하였습니다 (2015년 11월 27일 15시 50분. 제3회의장. 발표자 곽동신).
[2015-11-11. 김지현 교수님 편지]
제 개인적인 경험으로는 (추후 더 조사할 생각이지만) 분화형에서 cancer dedifferentiation에 의해 미분화형암이 생긴 경우에서는 어느 정도 술 전에 proximal margin clip시에 도움이 되었던 같습니다. 다시 한 번 제 연구 인용에 감사드리며, 즐겁고 행복한 하루 보내십시요.
 4. SRC 확대내시경 소견 - stretch sign
4. SRC 확대내시경 소견 - stretch sign
Showa 대학 팀에서 signet ring cell carcinoma의 NBI 확대내시경에 대한 짧은 논문을 발표하였습니다 (Phalanusitthepha C. WJGE 2015). 환자 수는 12명밖에 되지 않았습니다.
RESULTS: Twelve patients with early signet ring cell gastric carcinoma were identified; 75% were male, and average age was 61 years. Most of the lesions were stage T1a (83%), while the remainder were T1b (17%). The mean lesion size was 1.4 cm(2). On standard endoscopy, all 12 patients had a pale, flat lesion without any evidence of mucosal abnormality such as ulceration, elevation, or depression. On magnification endoscopy with NBI, all of the patients had irregularities in the glands and microvasculature consistent with early gastric cancer. In addition, all 12 patients exhibited the "stretch sign", an elongation or expansion of the architectural structure. Histologic examination of the resected specimens demonstrated an expanded and edematous mucosal layer infiltrated with tumor cells.
Gastric gland가 stretched 되어 보인다는 뜻인데요.... 그 기전을 아래와 같이 설명하고 있어서 흥미로웠습니다.
[Case 1 (위암 614)]
조기위암 expanded indication에 대한 논의가 활발합니다. 저는 분화형 점막암의 경우 size 기준을 flexible 하게 적용하고 있습니다만, 미분화 조직형암에 대해서는 매우 보수적인 입장을 가지고 있습니다. 1cm 이하 flat한 signet ring cell carcinoma 정도가 현재의 적응증입니다. 그에 해당하는 환자에 대하여 조심스럽게 시술하고 있습니다. 아직까지 이 기준에 해당하는 분 중에는 재발예는 없었습니다.
인근 병원에서 의뢰된 2016년 환자입니다. Signet ring cell carcinoma라는 조직진단이었습니다. 환자와 잘 상의 후 ESD를 진행하였습니다.
위암 내시경치료의 절대적응증은 점막에 국한된 궤양이 없는 2cm 이하의 분화형 조기위암입니다 (2012년 4월 1일 심평원). 이러한 기준을 벗어난 조기위암에 대해선 보통 수술을 권합니다. 그러나 기준을 약간 벗어난 병소에 대해서는 내시경치료를 시도해 보기도 합니다. 이를 확대적응증이라고 합니다.
과거에는 절대적응증을 확실하게 지켰습니다. 조금이라도 기준을 벗어나면 반드시 큰 수술을 받도록 권하는 방식이었습니다. 다만 고령이거나 심한 다른 장기 질환이 있어서 수술이 어려운 환자에서만 확대적응증에 대한 내시경 치료를 했습니다. 그 결과 작은 위암에 대해서도 큰 치료를 하는 셈이 되었고, 비록 암 재발률은 낮았지만 수술에 따른 합병증과 삶의 질 저하가 큰 문제가 되었습니다.
최근에는 절대적응증을 벗어난 위암이라도 세포형이 반지세포암 (signet ring cell carcinoma, 인환세포암)이고 크기가 작은 경우, 즉 확대적응증 중 그래도 내시경 치료를 할 수 있다고 생각되는 일부에 대해서는 아직 정부(심평원)에서 보험 급여로 인정하고 있는 부분은 아닙니다만 수술을 피하고 내시경 치료를 선택하기도 합니다. 일반적으로 절대적응증 내시경 치료 후 수술이 필요하다는 병리결과가 나오는 경우는 15%, 장기적인 재발률은 5% 수준입니다. 확대적응증은 이보다 조금 상회하는 수준일 것으로 생각하시면 되겠습니다. 대신 수술에 따른 합병증과 삶의 질 저하가 없다는 큰 장점이 있습니다.
시술은 무난하게 진행되었고 결과도 잘 나왔습니다.
(2016)
Posterior wall of proximal antrum, ESD : Early gastric carcinoma
1. Location : antrum, posterior wall
2. Gross type : EGC type IIc
3. Histologic type : signet ring cell carcinoma
4. Histologic type by Lauren : diffuse
5. Size of carcinoma : (1) longest diameter, 10 mm (2) vertical diameter, 6 mm
6. Depth of invasion : invades mucosa (lamina propria) (pT1a)
7. Resection margin : free from carcinoma(N), safety margin : distal 10 mm, proximal 16 mm, anterior 12 mm, posterior 8 mm, deep 1700 ㎛
8. Lymphatic invasion : not identified(N)
9. Venous invasion : not identified(N)
10. Perineural invasion : not identified(N)
11. Microscopic ulcer : absent
12. Histologic heterogeneity: absent
시술 관련하여 두 가지 이슈가 있습니다.
(1) 병소의 경계 판정입니다. 미분화 조직형 위암의 경우 병소의 경계가 모호하기 때문입니다. 시술 전 평가하였던 것보다 크게 나오는 경우도 많습니다. 이 환자도 5mm 정도로 생각했는데 실제로는 10mm로 나왔습니다. 따라서 미분화 조직형 위암의 내시경 치료 전 4 quadrant biopsy를 통하여 negative resection margin을 확보하려는 노력을 하기도 합니다. 그런데 이러한 노력은 무척 번거롭기도 하고 아직 그 효과가 100% 입증된 것도 아니므로, 시술자에 따른 선호도 차이가 크고, 병소에 따라서 불필요한 경우(예를 들어 육안 소견으로 경계가 비교적 명확해 보임 등)도 있습니다. 저는 거의 시행하지 않고 있습니다.
(2) 점막암의 내시경 치료라고 하더라도 가능하면 vertical margin을 충분히 확보하기 위하여 deep SM layer를 dissection 하고 있습니다. 미분화 조직형 암에서는 더욱 깊은 절제를 하기 위하여 노력을 합니다. 이 환자에서는 vertical resection margin (SM layer)가 1,700um로 비교적 넉넉하게 나왔습니다. 시술자로서는 아주 흡족한 결과입니다.
[Case 2]
2019년 signet ring cell carcinoma로 의뢰된 40대 여성입니다.
아직까지 SRC에 대한 ESD는 정식으로 보험급여가 되지 않고 있습니다. 선별급여인데요 치료비를 본인이 내는 것이라는 의미입니다. 따라서 우리나라 정부에서는 표준치료로 인정하고 있지는 않고 환자의 선택에 따라 시행할 수 있는 것 정도로 보는 상황입니다. 과잉 치료를 막는다는 측면에서 적절하다고 생각할 수 있지만 얼마 되지 않는 돈으로 환자나 의사의 선택권을 제한한다는 점에서 만족스럽지 않은 제도입니다. 그래서 저는 환자의 선택권을 존중한다는 차원에서 매우 자세히 설명을 합니다. 그리고 외래 후 의무기록을 복사하여 집에서 몇 번 읽어보도록 권하고 있습니다. 옮깁니다.
"위암으로 진단받고 예약하셨습니다.
몇 가지 검사는 필요합니다만... 전이 가능성이 매우 낮으므로 문제가 없다고 가정하고 설명하겠습니다.
치료 방법 선택이 중요합니다. 환자분의 경우는 조기위암이지만 미분화형이므로 내시경 치료의 절대적응증(표준적응증)에는 포함되지 않은 상황입니다.
위암 내시경치료의 절대적응증(표준적응증)은 점막에 국한된 궤양이 없는 2cm 이하의 분화형 조기위암입니다 (2012년 4월 1일 심평원). 이러한 기준을 벗어난 조기위암에 대해선 보통 수술을 권합니다. 그러나 기준을 약간 벗어난 병소에 대해서는 내시경치료를 시도해 보기도 합니다. 이를 확대적응증이라고 합니다.
과거에는 절대적응증(표준적응증)을 확실하게 지켰습니다. 조금이라도 기준을 벗어나면 반드시 큰 수술을 받도록 권하는 방식이었습니다. 다만 고령이거나 심한 다른 장기 질환이 있어서 수술이 어려운 환자에서만 확대적응증에 대한 내시경 치료를 했습니다. 그 결과 작은 위암에 대해서도 큰 치료를 하는 셈이 되었고, 비록 암 재발률은 낮았지만 수술에 따른 합병증과 삶의 질 저하가 큰 문제가 되었습니다.
최근에는 절대적응증을 벗어난 위암이라도 크기가 작은 경우, 즉 확대적응증 중 그래도 내시경 치료를 할 수 있다고 생각되는 일부에 대해서는 - 비록 아직 정부(심평원)에서 보험 급여로 인정하고 있는 부분은 아닙니다만 - 수술을 피하고 내시경 치료를 선택하기도 합니다. 일반적으로 절대적응증 내시경 치료 후 수술이 필요하다는 병리결과가 나오는 경우는 15%, 장기적인 재발률은 5% 수준입니다. 확대적응증은 이보다 조금 상회하는 수준일 것으로 생각하시면 되겠습니다.
시술방법은 내시경점막하절제술(ESD)입니다. 이를 위하여 3박 4일의 입원이 필요합니다. 준비시간을 제외하고 시술 자체에 소요되는 시간은 평균 45분입니다. 시술 도중 혹은 직후 급성 합병증으로 응급 수술이 필요한 경우는 0.1-0.2%입니다.
시술 후 약간의 복통이 가능하며 출혈과 천공 (=위벽에 작은 구멍이 남)이 5-6% 정도 발생합니다. 혹시 합병증이 있더라도 대부분 입원기간에 발생합니다. 퇴원 후 출혈하는 경우는 2-3%입니다.
내시경 시술 후 최종 병리결과는 1주일 후 외래에서 보실 수 있습니다. 분화조직형 위암에서는 7명 중 1명, 즉 15% 정도는 병리결과에서 세포형, 깊이, 범위, 림프관 침윤 등에 문제가 있어 수술이 필요하다고 나오고 7명 중 6명, 즉 85% 정도는 추가 치료가 필요없는 것으로 나옵니다. 미분화조직형 위암에서는 반지세포암(signet ring cell carcinoma)의 경우는 20% 정도, 저등급 분화형 위암 (poorly differentiated adenocarcinoma)에서는 30% 정도 수술이 필요하다고 나옵니다. 재발 위험이 높아서 수술(위절제술)이 필요하다고 나오면 외과로 입원하여 수술을 받게 됩니다. 간혹 암이라는 진단으로 내시경치료를 하였으나 단순 염증으로만 나오는 분도 있으나 그 빈도는 3%입니다.
시술 2개월 후 내시경 검사를 통하여 치료부위는 다 아물었는지, 잔류병소는 없는지 확인하여 문제가 없으면 더 이상 치료는 없습니다. 이후는 최소한 1년에 한번 이상 재검을 권합니다. 원래 병소가 재발하는 경우도 있지만, 첫 병소와 무관한 새로운 병소가 발견되는 경우도 많습니다.
현재 세 가지 정도의 어려움이 있습니다. (1) 최대한 빠른 진료를 위해 노력하고 있습니다만, 내시경절제술 대기환자가 무척 많습니다. 가장 빠른 시술일자를 잡아드리겠습니다. (2) 병원의 병실이 부족합니다. 간혹 예정된 입원일에 병실사정이 여의치 않을 수 있음을 양해하여 주시기 바랍니다. (3) 절대적응증이 아닌 경우 시술료 본인 부담으로 되어 있으나 그 비용은 정부에서 정해두었으므로 그다지 비싸지는 않습니다. 최종 조직검사 결과가 나온 후 약간 조정될 수 있습니다 (퇴원시 가수납). 저희는 규정에 어긋나지 않는 한 환자분께 경제적 부담이 되지 않도록 적절히 조처하겠다는 점을 약속드립니다.
확대적응증에 대한 시술에서는 환자분께 생각할 시간을 드리고 있습니다. 다음 주로 외래를 예약해 두겠습니다. 일단 시술 일자는 잡아두겠습니다.
내시경 시술을 시도할지, 수술을 시행할지에 따라 필요한 검사가 다르기 때문에 검사 처방은 다음 주에 하는 것이 좋겠습니다.
질문: 크기는 어떠합니까?
답변: 반지세포암은 크기를 정확히 측정하기 어려운 것으로 유명한 종류입니다. 현재 1cm 정도로 보이지만 내시경절제술이나 수술을 하여 현미경으로 확인해 보면 1cm인 경우도 있고 2cm 인 경우도 있고 3-4cm 인 경우 혹은 그 이상인 경우도 있습니다. 현재로서는 크기에 대하여 정확히 측정하기 어렵다고 보는 것이 좋겠습니다.
계획 1: 기본 검사
계획 2: 의무기록 복사
계획 3: 1주일 후 외래
계획 4: 내시경절제술(ESD) 예약"
1주일 후 외래에서 검사 결과를 확인하였고 전이 소견은 없었습니다. 환자는 가족들과 충분히 상의했다고 말하였고 ESD를 원하였습니다. 입원 후 시술하였습니다.
퇴원 후 다음 주 외래에서 결과를 확인했습니다.
병리 세미나에서 제 눈으로 병소를 확인했습니다. Lamina propria에 국한된 전형적인 signet ring cell carcinoma였습니다. 점막층 하단에는 lymphocyte/plasma cell infiltration이 현저하고 lymphoid follicle이 dense하게 관찰되고 있었습니다. 역시 Helicobacter가 범인 같습니다. 나쁜 녀석 같으니라고.... 병리 결과를 보고 안심하였지만 직접 눈으로 보이 더욱 확신이 들었습니다.
Signet ring cell carcinoma 환자 한 명을 치료하기 위해서는 정말 많은 정신력과 노동이 필요합니다. 힘든 일입니다.
[Case 3]
SRC로 ESD 후 점막암 병리학적 완전절제였지만 1.7cm이고 뚜렷한 함몰형이므로 수술적 치료를 권유받고 이차 의견 위하여 의뢰되었습니다. 저도 수술을 권하였습니다. 시술자가 수술을 권하는데 다른 의사가 경과관찰을 권하기는 거의 불가능한 상황입니다.
[Case 4]
Signet ring cell carcinoma입니다. 생각보다 범위가 넓을 수 있다는 점에 주의하시기 바랍니다. 주변의 퇴색부까지 전부 암입니다 (노란색 화살표).
재검 후 fold 변화가 현저한 점이 특징이었습니다. 조직검사 후 fold 모양이 바뀔 수 있습니다. 없던 것이 생길 수도 있습니다.
최종 결과는 아래와 같았습니다.
Stomach, radical subtotal gastrectomy: Early gastric carcinoma
1. Location : middle third, Center at proximal antrum and greater curvature
2. Gross type : EGC type IIc
3. Histologic type : signet-ring cell carcinoma
4. Histologic type by Lauren : diffuse
5. Size : 4.0x2.5 cm
6. Depth of invasion : invades submucosa (sm1) (pT1b)
7. Resection margin: free from carcinoma, safety margin: proximal 5.0 cm, distal 5.3 cm
8. Lymph node metastasis : no metastasis in 58 regional lymph nodes (pN0)
9. Lymphatic invasion : not identified
10. Venous invasion : not identified
11. Perineural invasion : not identified
12. AJCC stage by 8th edition: pT1b N0
[2014년 대토론]
[2014-9-30. 애독자 질문]
최근 저희 병원 병리 선생님들은 signet ring cell cancer를 poorly cohesive cancer라고 혼용해서 주는 경향이 있습니다. 그래서 물어봤더니 이 두가지 개념이 완전히 일치하지는 않는다고 하더군요. 그냥 지금은 혼용해서 쓸수 밖에 없다고 하는데 선생님 생각은 어떠신지요?
[2014-9-30. 이준행 답변]
맞습니다. 무척 헷갈리는 일입니다. 위암 분화도에는 헷갈리는 이슈가 무척 많습니다. 일전에 정리한 내용은 아래와 같습니다. Signet ring이 뚜렷하게 보이면 SRC이고 그렇지 않으면 SRC를 포함하는 보다 넓은 개념인 poorly cohesive라고 준다는 정도로 알고 있는데요..... 제가 몇 분 병리선생님께 문의하여 얻은 답변을 소개합니다.
위암병리판독의 기준으로 간주되는 2005년 대한병리학회 소화기병리학연구회의 위암 병리보고서 기재사항 표준화 (PDF 0.3M)에는 (1) 위암의 histologic type은 2000년 WHO 분류를 따름, (2) 두 가지 이상의 분화도가 섞여 나올 때는 간질을 제외한 암세포의 면적이 가장 많은 유형으로 분류함, (3) 선구조나 편평상피 분화가 없는 경우에는 undifferentiated carcinoma로 분류함을 명확히 밝히고 있습니다.
위에서 언급한 2005년 병리 표준안에서는 2000년 WHO 분류를 따른다고 되어 있습니다. 그런데 2010년 WHO 4판 분류가 나왔고, 위암의 조직형은 다음과 같이 바뀌었습니다. 그러니까 2014년 현재의 국제 표준입니다. 가장 큰 차이는 poorly cohesive carcinoma가 추가된 것이고 그 의미는 아래 screenshot과 같습니다.
8140/3 Adenocarcinoma, NOS
- 8260/3 Papillary adenocarcinoma, NOS
- 8211/3 Tubular adenocarcinoma
- 8480/3 Mucinous adenocarcinoma
- 8490/3 Poorly cohesive carcinoma, including signet ring cell carcinoma and other variants
- 8255/3 Adenocarcinoma with mixed subtypes
8560/3 Adenosquamous carcinoma
8512/3 Medullary carcinoma with lymphoid stroma
8576/3 Hepatoid carcinoma
8070/3 Squamous cell carcinoma, NOS
8020/3 Undifferentiated carcinoma
[2014-9-30. 병리 교수님 1 답변]
WHO 분류 4판에 소개된 Poorly cohesive carcinoma는 signet ring cell carcinoma를 포함하는 개념입니다. 암종세포는 다른 세포에 비하여 세포간의 응집력이 높기 때문에 서로 뭉쳐서 특정 구조를 만드는 것이 일반적인 특징입니다. 그러나 저분화 암종 (poorly differentiated carcinoma) 중에는 암종세포 간에 응집력이 떨어져서 서로 뭉치지 않는 형태를 보이는 경우가 있는데, 이를 통칭하여 poorly cohesive carcinoma라고 합니다. 이를 구성하는 각각의 암종세포를 형태학적으로 살펴보면, 반지모양 세포 (signet ring cell)인 경우가 가장 흔하지만, 그 외에도 조직구 (histiocyte)나 림프구 (lymphocyte)를 닮은 경우도 있습니다. 따라서 조직학적으로 응집력이 떨어지는 저분화 암종이 관찰될 때, 그 구성세포의 50%이상이 반지모양을 취하는 경우에는 Signet ring cell carcinoma로, 다른 형태가 더 우세한 경우에는 poorly cohesive carcinoma로 진단하게 됩니다.
[2014-9-30. 이준행의 추가 질문과 병리과 교수님 1의 답변]
1) 이준행 질문: WHO 4판을 통하여 poorly cohesive carcinoma라는 분류가 도입되기 이전에 "조직학적으로 응집력이 떨어지는 저분화 암종에서 구성세포의 50%이상이 반지모양을 취하는 경우(Signet ring cell carcinoma)가 아닌 증례", 다시 말하면 50% 이하의 signet ring cell carcinoma가 있는 응집력이 떨어지는 저분화암종은 어떻게 불리었는지 궁금합니다.
병리과 교수님 답변: 이 답변은 문헌에 근거하기 보다는 제 경험과 추측에 의한 것이라는 전제를 드립니다. 선생님께서 말씀하시는 "50% 이하의 signet ring cell carcinoma가 있는 응집력이 떨어지는 저분화암종"의 경우의 대부분은 signet ring cell carcinoma로 진단되었을 가능성이 가장 높습니다. 왜냐하면 2000년 WHO의 signet ring cell carcinoma의 형태학적 기술을 읽어보면 지금의 poorly cohesive carcinoma와 그리 다르지 않기 때문입니다 (2010년에는 세포형태학적으로 signet ring cell morphology가 아닌 것들을 포함할 수 있는 "poorly cohesive carcinoma"라는 용어를 하나 만든 것 같습니다). 그러나 일부는 poorly differentiated adenocarcinoma로 진단되었을 가능성도 있습니다. 왜냐하면 응집력은 떨어지지만 종양세포가 빽빽하게 들어 차 있는 경우는 poorly differentiated adenocarcinoma, solid type과 구분이 어렵기 때문입니다. 또한 signet ring cell carcinoma나 poorly differentiated adenocarcinoma가 모두 diffuse type (undifferentiated type)에 속하기 때문에 반드시 구분할 필요성이 없다고 생각한 면도 없지 않습니다.
2) 이준행 질문: WHO 4판을 통하여 poorly cohesive carcinoma라는 분류가 도입되기 이전에 poorly differentiated adenocarcinoma라고 분류되는 것 중 어느 정도는 아직도 poorly differentiated adenocarcinoma로 불리고 어느 정도는 poorly cohesive carcinoma라고 불리고 있는지요?
병리과 교수님 답변: 어느 정도라고는 단정지을 수는 없으나 두가지 진단이 다 쓰일 것으로 생각됩니다. 윗 질문에 답과 어느 정도 겹치는 것 같습니다.
3) 이준행 질문: 언뜻 생각하기게 mucinious adenocarcinoma도 poorly cohesive한 성격을 가진 것들이 종종 있을 것 같습니다. 어떻게 이해하여야 하올지 궁금합니다.
병리과 교수님 답변: Mucinous adenocarcinoma를 다시 low grade (differentiated type)과 high grade(undifferentiated type)으로 나눌 수 있습니다. Extracellular mucin을 제외한 종양세포의 형태가 말씀하신 것처럼 poorly cohesive, signet ring cell의 형태를 띄는 경우는 high grade (undifferentiated type)으로 분류됩니다.
[2014-10-1. 병리 교수님 2 답변]
답변: Poorly cohesive carcinoma는 2010년에 개정된 WHO classification of digestive system에 새로이 등장한 용어입니다.현미경 소견상 adenocarcinoma이지만 종양세포들이 gland를 만들기 보다는 낱개 또는 작은 군집을 형성하는 경우를 통칭하는 분류입니다. 이 중 종양세포 모양이 반지 모양인 경우가 signet rign cell carcinoma이고 가장 대표적이지만, 이외에도 종양세포 모양이 histiocyte나 lymphocyte처럼 생긴 경우도 있고, 아주 bizarre/pleomorphic cell로 구성된 예도 이에 포함되기 때문에 동일어는 아니고 포괄적인 용어라고 생각해야 할 것 같네요. WHO blue book에는 adenocarcinoma의 조직학적 아형중 하나로 poorly cohesive carcinoma, including signet ring cell carcinoma and other variant로 나와 있습니다.
[2014-10-1. 병리 교수님 3 답변]
signet ring cell carcinoma는 poorly cohesive carcinoma의 한 유형입니다. 병리학회 지침서에는 WHO classification을 따르도록 권유하고 있구요, 저는 2010년 WHO classification에 따라 진단 용어를 쓰고 있습니다.
[2014-10-1. 병리 교수님 4 답변]
아시다시피 2010년 WHO blue book (제가 "신주단지" 로 표현하고 선생님께서 화답해 주셨던 책입니다^^) 이 개정되었습니다. Adenocarcinoma 분류가 달라진 점은 아래와 같습니다.
2010 이전판 Adenocarcinoma
- Papillary
- Tubular
- Mucinous
- Signet ring cell2010 판 Adenocarcinoma
- Papillary
- Tubular
- Mucinous
- Poorly cohesive (including signet ring cell carcinoma and other variants)즉 얼핏보면 signet ring cell 대신 poorly cohesive가 들어가서 둘이 같은 것인가 싶지만 괄호안을 보면 poorly cohesive에 signet ring 및 또 다른 것이 포함된 것임을 알 수 있고 완전 동의어가 아님을 알 수 있습니다. Poorly cohesive carcinoma에 포함되는 다른 형태로는 histiocyte 나 lymphocyte 를 닮은 cancer (hematopoietic 세포는 cohesiveness 가 없습니다) deeply eosinophilic cytoplasma을 보이거나 irregular bizarre nuclei를 보이면서 cohesive하지 않은, 그렇지만 signet ring cell 모양을 나타내지 않는 cancer가 포함됩니다. 하지만 워낙 signet ring cell carcinoma가 뚜렷하게 각인된 type이다보니 signet ring cell carcinoma로 쓰기도 하고 poorly cohesive carcinoma로 쓰기도 하는 것 같습니다.
저의 경우는 signet ring cell carcinoma는 그냥 signet ring cell carcinoma로 쓰고 signet ring 에 또 다른 poorly cohesive carcinoma가 많이 섞이거나 signet ring 이 아닌 다른 poorly cohesive carcinoma일때는 poorly cohesive로 쓰고 있습니다. 그런데 어떤 선생님은 signet ring cell carcinoma를 아예 poorly cohesive carcinoma 로 진단하시기도 하더라고요.
WHO 에서 변화가 있으니 그에 따라야겠지만 제 생각에도 좀 더 친절하게 분류를 해주면 좋겠다 싶습니다. 어쩌면 다음판에는 poorly cohesive carcinoma, signet rin cell type 과 poorly cohesive carcinoma, NOS type으로 분류가 될지도 모르겠습니다. 제탓은 아니지만 죄송합니다.ㅠㅠ 좋은 하루 되세요^^
[2014-10-1. 병리 교수님 5 답변]
Poorly cohesive carcinoma는 signet ring cell carcinoma를 포함하는 개념으로 새로 바뀐 WHO classification 2010에 새롭게 등장한 용어입니다. 대부분의 carcinoma는 세포끼리 서로 붙어있는 것이 특징인데, signet ring cell carcinoma를 포함 일부에서는 이런 특징을 잃어 버리고 일부 e-cadherin의 발현이 없어지게 됩니다.
Signet ring cell carcinoma 외에도 lymphocyte 혹은 histiocyte를 닮은 종양세포나 eosinophilic cytoplasm을 가진 세포들, 혹은 irregular, bizzare nuclei를 가진 세포들이 pooly cohesive하게 분포할 때를 언급하는 말입니다. 이 용어는 아직 많은 병리의사에게 생소하며 많은 병리의사의 지지를 받는다고는 할 수 없을 듯 합니다. 단, 지금 WHO 분류체계에서 signet ring cell carcinoma가 여기에 포함되므로 불가피하게 용어를 사용하고 계신다고 생각됩니다.
[2014-10-1. 토론을 지켜본 내과 교수님 comment]
제가 병리 전문가가 아닌 입장에서 뭐라 토를 달기가 어렵습니다. 다만, 내시경 의사들이 병리 의사들의 진단기준을 조금 더 존중했으면 하는 바램입니다. 병리과에서 poorly-cohesive로 통일했음에도 불구하고, signet ring cell carcinoma (SRCC)로 마음대로 바꿔서 발표하는 소화기내과 의사들이 없었으면 좋겠습니다.
[2014-10. 2014년 대토론에 대한 이준행 총평]
저는 늘 고민합니다. "우리 기준이 있고 WHO 기준이 있을 때 어느 것을 따를 것인가?" 우리 기준과 WHO 기준이 동시에 바뀌는 법은 없습니다. 보통 WHO 기준이 먼저 바뀌고 나중에 우리 현실을 반영한 새로운 우리 기준이 나옵니다. 그 사이가 문제입니다. WHO에서는 용어를 바꿨는데 우리는 아직 안 바꾼 상황에서 WHO 용어를 써야 할까요, (다소 낡았지만 그래도) 우리 용어를 써야 할까요? WHO 기준이 바뀌면 즉시 사용하는 선생님이 계신가 하면 우리 기준이 바뀌기 전까지는 원래 용어 그대로 사용하는 분도 계십니다. 여러분은 어떤 생각이십니까?
저는 단순명료한 것을 좋아합니다. 기준은 하나여야 합니다. 결정하면 됩니다. WHO 기준을 쓸 것인지 우리 것을 쓸 것인지 우리가 정하면 됩니다. 만약 WHO 기준을 따르기로 했으면 우리 기준은 만들지 않는 것이 좋습니다. 꼭 만들어야 한다면 "우리나라에서 이 분야는 WHO 기준을 따른다"라는 한 마디로 끝내야 합니다. 만약 우리 기준을 만들어 사용하기로 했으면 WHO 기준이 바뀌더라도 우리는 우리 기준을 따라야 합니다. 다소 낡았더라도 새로운 우리 기준이 나오기 전까지는 우리 기준을 고수해야 합니다. 당연하지 않습니까?
(참고로 미국 기준과 WHO 기준을 혼동하면 안 됩니다. 미국 기준은 미국에서 사용하는 기준이고 WHO 기준은 국제기준입니다. 간혹 미국 기준이 바뀌었다고 우리도 용어를 바꿔야 한다고 주장하는 분도 계시는데 저로서는 이해할 수 없습니다. 우리가 미국 식민지입니까? 미국 기준 가지고 와서 이렇다 저렇다 이야기하는 행동은 이제 그만 합시다.)
이런 문제의식이 없는 상태에서 일단 우리는 우리의 기준을 만들었습니다. 그리고 WHO를 쓸 것인지 우리 것을 쓸 것인지 명확히 정하지 않은 상태에서 오랜 시간이 지나갔습니다. 사실 별 문제가 없었습니다. 전판 WHO 기준과 우리 기준이 같았기 때문입니다. 많은 분들이 잘 몰랐습니다. 우리 기준을 쓰고 있던 것인지 WHO 기준을 쓰고 있던 것인지 본인 스스로 명확하지 않았습니다. 논리적으로는 우리 기준을 쓰고 있던 것인데 - 우리 기준을 만든 것 자체가 우리 기준을 쓰겠다는 의미입니다 - 많은 사람들은 WHO 기준을 쓰고 있다고 착각했던 것입니다. 그런데 갑자기 WHO 기준이 변경되었습니다. 혼란이 올 수 밖에 없습니다. 우리 기준을 쓰고 있다고 생각하던 사람은 신판 WHO 기준 용어를 받아들이지 않았고, WHO 기준을 쓰고 있다고 생각하던 사람은 재빨리 신판 용어로 변경하였습니다. 대혼란이 벌어졌습니다.
참고로 2014년 위암 가이드라인의 병리 부분은 아래와 같습니다.136번 참고문헌은 2010년 WHO 기준입니다. 적어도 위암 가이드라인에서는 2010년 WHO 기준에 따른 분류를 채택하고 있는 셈입니다. 그렇다면 위암 가이드라인은 모든 병리의사들이 따라야하는 표준안으로 받아들여졌을까요? 저도 잘 모르겠습니다. 병리학회의 추인은 받았지만 회원들이 모두 잘 알고 있는지는 가이드라인 제1 저자인 저 자신도 확신할 수 없습니다.
WHO 기준도 좋고 우리 기준도 좋습니다. 우리 환자에게 도움되면 그만이고, 환자를 치료하는 의사들이 헷갈리지 않으면 그만입니다. 부디 쉽고 편리한 방향으로 정리되기를 바랄 뿐입니다. 제가 파악하기로는 2010년 WHO 분류가 2014년 현재 대한민국 병리 용어의 표준인 것 같습니다. 모든 병리과 의사들이 이 용어로 통일된 보고서를 내 줄 것을 바랄 뿐입니다. 그리고 한 내과 선생님께서 지적한 바와 같이 병리과 선생님의 진단명을 내과의사가 자의적으로 변경하여 사용하지 말았으면 합니다.
정리합니다. 병리 의사는 표준안을 하나 정하여 모두 따라주면 좋겠고, 내과 의사는 병리 의사의 용어를 존중하면 좋겠습니다.
교수님 안녕하십니까. EndoTODAY 홈페이지 잘 보고 있습니다. 작성해주신 글들 뿐 아니라 애독자 질문도 공유해주신 덕분에 진행되었던 토의들, 다른 분들의 의견들을 보면서 배울 수 있는 점 감사합니다. 다름이 아니라 다음 글들 보고 질문이 생겨서 메일 드려봅니다. http://endotoday.com/endotoday/src.html#2014
Signet ring cell carcinoma 판독 소견이 나오면 적응증 여부에 따라 내시경 치료나 외과 외래로 의뢰합니다.
1. 최근 논문들을 보면 내시경 치료 후 조직검사 결과가 non-neoplastic인 경우가 있습니다. http://endotoday.com/endotoday/esd_nonneoplastic.html에서도 소개해 주셨습니다.
(1) Predictive Model of Nonneoplastic Pathology after Endoscopic Resection of Gastric Epithelial Neoplasia: The rate of nonneoplastic pathology (NNP) after endoscopic resection (ER) of gastric epithelial neoplasia (GEN) has been reported to be 3%?7%.
(2) Non-neoplastic pathology results after endoscopic submucosal dissection for gastric epithelial dysplasia or early gastric cancer: The ESD specimens included 52 (4.4 %) that were confirmed as negative or indefinite for neoplasia.
(3) Clinical outcomes of no residual disease in the specimen after endoscopic resection for gastric neoplasms : NRD was detected in 143 (3.2%) of 4401 cases of gastric neoplasms treated with ER.
2. signet ring cell cancer pathology 관련하여 좀 더 찾다보니 signet ring cell change가 signet ring cell carcinoma 소견을 mimicking 하는 경우가 있다고 보고한 케이스들이 있었습니다 (Mimickers in GI pathology - PDF).
(1) Nonneoplastic signet-ring cell change in gastrointestinal and biliary tracts: a pitfall for overdiagnosis : Nonneoplastic signet-ring cell change (SRCC) is a rare but known phenomenon in gastrointestinal and biliary tracts and is always associated with underlying mucosal ulceration/erosion secondary to infection, ischemia, or other etiology. Because nonneoplastic SRCC closely mimics signet-ring cell adenocarcinoma (SRCA), differentiation of these 2 entities is critical because misdiagnosis of nonneoplastic SRCC as SRCA can lead to intense therapeutic interventions such as surgery and/or chemoradiation therapy. In this review, a brief overview on nonneoplastic SRCC in gastrointestinal and biliary tracts, including the spectrum of clinical presentation, important histologic features, and immunohistochemical markers that are useful in differentiating nonneoplastic SRCC from SRCA, is provided. The pathogenesis of nonneoplastic SRCC in gastrointestinal and biliary tracts is discussed.
(2) Reticulin staining clarifies florid benign signet ring cell change with mitotic activity in a penetrating gastric ulcer : Signet ring cell change is a benign process that can be mistaken for signet ring cell adenocarcinoma. Signet ring cell change remains confined within the basement membrane and lacks an infiltrative growth pattern. It typically lacks cellular atypia, nuclear hyperchromasia, prominent nucleoli, or mitotic activity. This study illustrates a case of signet ring cell change with mitotic activity in a background of Helicobacter pylori gastritis with a penetrating ulcer.
(3) Signet-ring cell change versus signet-ring cell carcinoma: a comparative analysis : Signet-ring cell change (SCC) is a nonneoplastic condition that morphologically simulates signet-ring cell carcinoma (SRCA). The few case reports on SCC have focused on morphologic characteristics in distinguishing benign from malignant. In biopsy specimens, however, SCC can be easily confused with SRCA, which often demonstrates innocuous cytologic features. Cells in SCC were strongly positive for E-cadherin and negative for p53 and Ki-67. In contrast, cells in SRCA were strongly positive for p53, exhibited high proliferation, and demonstrated absent or weak positivity for E-cadherin.
3. 내시경 치료 후 조직검사 결과가 non-neoplastic인 경우가 보고되고 있고, 면역조직화학검사 (Reticulin, p53, Ki-67, and E-cadherin)를 처방하는 경우가 드문 현실에서 조기 위암 biopsy (signet ring cell carcinoma) 판독 소견 확인하신 후 (병리과 선생님께서 권유하시는 경우도 드문 듯 합니다.) 추가 처방으로 위양성(misdiagnosis or over-diagnosis)이 아님을 확인해 보시는 경우도 있으신지 고견이 궁금합니다. 현실적으로 근거는 부족하지만 상황에 따라 환자 동의 있는 경우 시도해 볼 필요도 있을까 하여 문의드립니다.
바쁘신 중에 긴 글 읽어주셔서 감사합니다. 건강하고 즐거운 봄날 보내시길 바랍니다.
[2021-5-2. 이준행 답변]
Signet ring cell carcinoma와 비슷할 수 있는 signet ring cell change를 암진료 현장에서는 어떻게 하고 있는지 문의하여 주셔서 감사합니다.
내시경 조직검사의 sensitivity가 100%가 아니라는 것은 누구나 알고 있습니다. 암이 의심되는데 조직검사에서 암이 나오지 않으면 즉시 혹은 short-term follow-up biopsy를 합니다. 내시경 조직검사의 specificity도 100%가 아닙니다. 암이라고 나왔어도 암이 아닌 경우가 있습니다. 이는 비단 signet ring cell carcinoma에만 해당하는 것은 아니고 다른 모든 암도 마찬가지입니다.
조직검사에서 암이 나왔더라도 내시경 소견이 암 같지 않으면 합리적인 의심을 해야 합니다. 이 때 크게 고려하는 것이 치료방법입니다. Subtotal gastrectomy처럼 크고 비가역적인 치료를 해야 하는 상황에서는 진단의 정확성이 100%에 근접해야 합니다. 그러나 ESD나 H. pylori 제균치료처럼 혹시 약간의 과잉치료가 되었더라도 환자에게 남는 위해가 크지 않는 경우는 진단의 정확도가 다소 낮더라도 치료를 시작할 수 있습니다.
1. 조직검사에서 암으로 의뢰된 환자에서 수술이 필요한 경우에는 내시경 조직검사를 재검하여 다시 한 번 조직학적 암진단을 확인한 후 수술을 하고 있습니다.
2. 조직검사에서 암으로 의뢰된 환자에서 ESD가 필요한 경우에는 내시경 조직검사 재검을 하지 않고 외부 슬라이드 재판독 후 ESD를 하고 있습니다.
3. 간혹 외부 조직검사에서 암으로 나왔으나 의뢰 후 재검에서 암으로 나오지 않는 경우는 다시 한번 내시경 조직검사를 하고 있습니다. 이 이슈에 대해서는 개인적으로 관심이 있어서 2016년 Negative biopsy after referral for biopsy-proven gastric cancer라는 제목으로 발표한 바 있습니다. 아주 여러번 추적검사를 해도 암으로 나오지 않는 분이 분명 계십니다. 그 이유 중 하나가 biopsy false positive일 것이며 signet ring cell change도 그 원인 중 하나일 수 있다고 생각합니다.
결국 내시경 소견이 조직검사 결과와 어울리는지 조심스럽게 살피는 수 밖에 다른 도리가 없습니다. 이런 관점에서 내시경을 배우지 못한 의사가 (건진 같은 곳에서) 조직검사 결과를 판정하는 현실이 매우 걱정스럽습니다. 내시경 조직검사 결과 판정은 내시경 specialist의 역할입니다.
Signet ring cell carcinoma가 의심되지만 확실하지 않다고 의뢰된 환자로 제균치료를 하였고 이후 수차례 조직검사에서도 암이 나오지 않았음
[2022-1-16. 이준행 추가] 2000판 WHO tumours of the digestive system 44쪽에서 이런 언급을 보았습니다. "Several conditions mimic signet-ring cell carcinoma including signet-ring lymphoma, lamina propria muciphages, xanthomas and detached or dying cells associated with gastritis."
[2026-3-1. 추가] 해외에서 출혈로 내원하여 내시경 조직검사 결과 adenocarcinoma diffuse infiltrative로 수술을 하였는데 최종 병리 결과 암이 나오지 않았던 증례. 위암 조직검사도 위양성(biopsy false positive)이 가능함을 보여주는 증례라고 생각됩니다.
 [2024-12-27] 제29회 병리세미나를 금요내시경집담회와 통합하여 진행하였습니다. 그간 안수민 교수님과 저의 개인 교습 스타일로 진행해왔었고 가끔 다른 교수님들이나 fellow들이 함께 한 적은 있습니다. 그러나 모든 분들에게 도움될 것으로 판단되어 처음으로 병리과 선생님을 모신 regular 병리집담회를 시작하였습니다. 20년 전부터 하고 싶던 것을 드디어 성사시켜 매우 기쁩니다.
[2024-12-27] 제29회 병리세미나를 금요내시경집담회와 통합하여 진행하였습니다. 그간 안수민 교수님과 저의 개인 교습 스타일로 진행해왔었고 가끔 다른 교수님들이나 fellow들이 함께 한 적은 있습니다. 그러나 모든 분들에게 도움될 것으로 판단되어 처음으로 병리과 선생님을 모신 regular 병리집담회를 시작하였습니다. 20년 전부터 하고 싶던 것을 드디어 성사시켜 매우 기쁩니다.
Signet ring cell carcinoma도 두 종류가 있다는 것이 저의 주장입니다. Hp negative이고 flat 하고 white 하고 예후가 매우 좋은 것과 Hp positive이고 AGC가 되기 쉽고 재발이 많은 종류입니다. 이 개념을 좀 더 연구해 볼 생각입니다.
© 일원내시경교실 바른내시경연구소 이준행. EndoTODAY Endoscopy Learning Center. Lee Jun Haeng.