 EndoTODAY 내시경 교실
EndoTODAY 내시경 교실
Parasite | Eso | Sto | Cancer | ESD
 [Tips for EMR/ESD (천기누설)] - 終
[Tips for EMR/ESD (천기누설)] - 終
"기술은 예술을 필요로 하지 않는다. 그러나 예술은 기술을 필요로 한다."
Walter Gropius
6. FAQs
8. References
치료내시경에서는 사소한 기술적인 문제가 중요한 경우가 많습니다. 그러나 구체적인 내용은 어느 교과서나 저널을 찾아봐도 잘 나와있지 않습니다. 학술회의장에서 어렵게 질문을 하더라도 "그런 구체적인 문제는 강의가 끝난 후 개별적으로 질문하여 주십시요"라는 말과 함께 따가운 눈총을 받기도 합니다. 그러나 개인적 친분이 없는 강사에게 1:1로 질문하는 것은 쉬운 일은 아닙니다.
혹자는 기술적 detail을 자신의 비법으로 생각합니다. 유교문화의 영향으로 기술적인 문제를 공개적으로 논하는 것은 품위가 떨어지는 일로 간주하기도 합니다. 이러한 경향은 외과보다 내과에서 심합니다. 그러나 기술적 detail은 매우 중요한 지식입니다. 이론적 지식 못지 않게 중요합니다.
저는 2005년 지식의 공유가 의학발전에 기여한다는 신념하에 치료내시경과 관련된 tip을 소개하는 "천기누설" 코너를 열었습니다. 6년이 지났기 때문에 대대적 upgrade를 계획하고 있습니다. 많은 관심을 부탁합니다.
본 코너에서 제시된 내용은 치료내시경의 절대적 가이드라인은 아니며 단지 개인적 의견임을 밝힙니다.
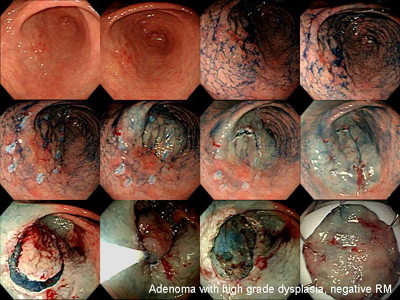
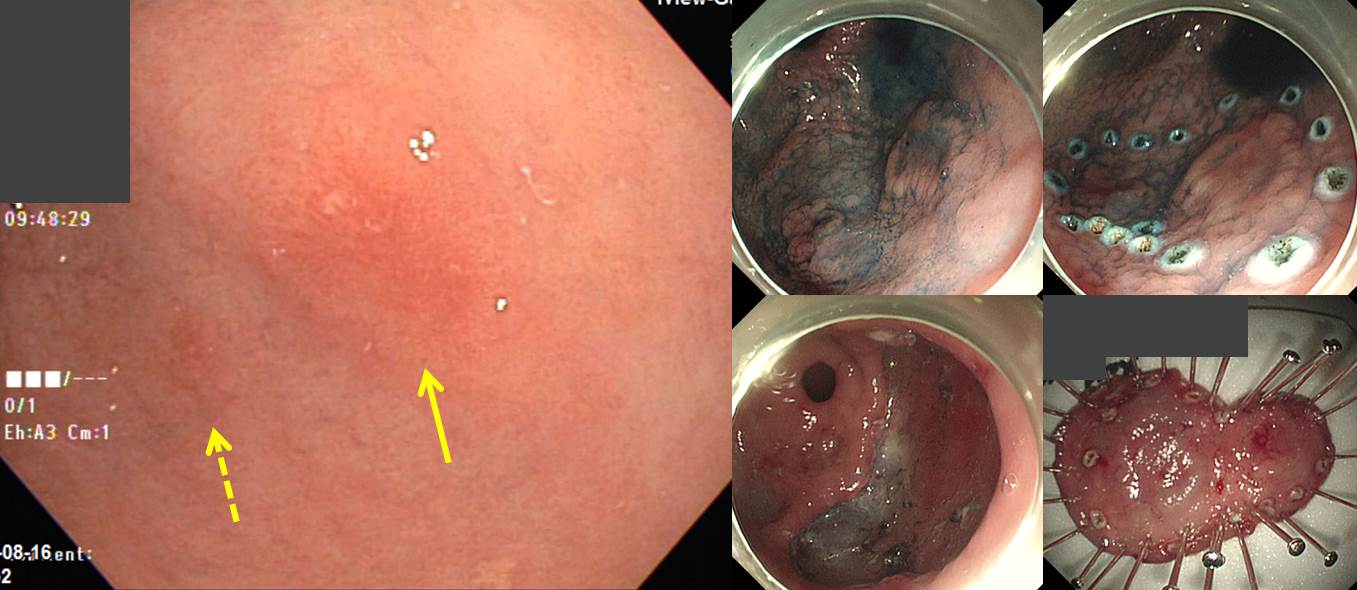 타 의료기관에서 내시경 및 조직검사로 진단된 선종이나 조기위암 환자의 내시경 치료 전 내시경 재검이 필요할까요? 저는 첫 내시경 사진을 검토하여 검사가 적절히 이루어졌고 병소에 대한 명확한 사진이 있으면 재검하지 않고 즉시 시술을 하고 있습니다. 그 과정 중 종종 추가 병변이 발견됩니다. 다행스럽게 첫 병소와 추가 병소가 매우 가까우면 한꺼번에 절제하기도 합니다. 고도선종으로 의뢰된 환자입니다. ESD를 하기 직전 추가 병소를 발견하였는데, 두 병소의 위치가 매우 가까워 한꺼번에 치료하였고 최종 병리결과도 잘 나왔습니다. "Tubular adenoma with high grade dysplasia. (1) 14 x 13 mm, (2) 10 x 8 mm, negative resection margins." 그런데 처음 사진을 자세히 살펴보니 두번째 병소가 희미하게 보였습니다 (노란 점선 화살표). 아래 증례도 거의 동일한 경우였습니다. [2017-9-10]
타 의료기관에서 내시경 및 조직검사로 진단된 선종이나 조기위암 환자의 내시경 치료 전 내시경 재검이 필요할까요? 저는 첫 내시경 사진을 검토하여 검사가 적절히 이루어졌고 병소에 대한 명확한 사진이 있으면 재검하지 않고 즉시 시술을 하고 있습니다. 그 과정 중 종종 추가 병변이 발견됩니다. 다행스럽게 첫 병소와 추가 병소가 매우 가까우면 한꺼번에 절제하기도 합니다. 고도선종으로 의뢰된 환자입니다. ESD를 하기 직전 추가 병소를 발견하였는데, 두 병소의 위치가 매우 가까워 한꺼번에 치료하였고 최종 병리결과도 잘 나왔습니다. "Tubular adenoma with high grade dysplasia. (1) 14 x 13 mm, (2) 10 x 8 mm, negative resection margins." 그런데 처음 사진을 자세히 살펴보니 두번째 병소가 희미하게 보였습니다 (노란 점선 화살표). 아래 증례도 거의 동일한 경우였습니다. [2017-9-10]
전신마취를 이용하려면 많은 장비와 인력이 필요합니다. 마취과 의사과 마취 간호사가 필요합니다. 저는 Midazolam만을 사용하고 있습니다.
내시경을 이용한 용종, 선종, 위암의 치료법은 매우 다양하지만 크게 ablation method와 tissue retrieval method로 나눌 수 있습니다. Tissue retrieval method는 위와 같이 suction을 이용하는 방법과 이용하지 않는 방법이 있습니다. 제가 주로 사용하는 방법은 Inject and cut method, EMR-P와 endoscopic submucosal dissection (ESD)입니다. Inject and cut method는 hyperplastic polyp의 제거, EMR-P는 작은 선종의 치료, ESD는 큰 선종이나 조기위암의 치료에 주로 이용하고 있습니다. 각각의 방법은 나름대로의 장단점이 있으므로 이 중에서 몇가지 방법을 자유자재로 구사할 수 있는 능력을 갖추는 것이 무엇보다도 중요하다고 할 수 있습니다. [2005-2-1. 이준행]
ESD는 기존의 EMR에 비하여 시술의 난이도가 높고 사용하는 장비가 다르며, 시술시간이 오래걸리는 등의 차이가 있으므로 기존의 EMR과 다른 새로운 시술로 간주하는 것이 일반적이다. EMR과 ESD를 합한 개념은 ER (endoscopic resection)으로 부르기도 한다. [2006-5-25. 이준행]
2010년 여자 환자입니다. 위각부의 조기위암이 발견되었고 multiple EMR-C (two pieces)가 시행되었으며, moderately differentiated adenocarcinoma 점막암(lamina propria)이었으나 resection magin positive로 나와 추가 치료를 위하여 의뢰되었습니다. 내시경 재검 ESD ulcer 조직검사에서 잔류암이 있는 것으로 확인되었습니다. 수술적 절제가 표준적인 치료이지만 내시경 치료도 고려해 볼 수 있는 상황이었습니다. 처음부터 ESD를 했더라면 충분히 resection margin negative complete resection을 만들 수 있었을 것으로 판단되었습니다. ESD를 배우고 익혔더라면 좋지 않았을까요? EMR-C는 lateral margin negative complete resection을 만들기 어렵기 때문에 최근에는 거의 사용하지 않는 방법입니다. [2010-1-2. 이준행]
가천 길병원 정준원 교수님께서는 2015년 12월 Gastrointestinal Endoscopy에 위 ESD에서 room air 대신 CO2를 사용하면 시술 후 복통이 적다는 무작위대조군연구를 발표하셨습니다 (Kim SY. GIE 2015). CO2는 주로 대장내시경에서 사용되고 있는데, room air 보다 좋은 이유는 위장관에서 혈액으로 흡수되어 폐를 통하여 배출되는 속도가 빠르기 때문입니다.
저는 CO2를 사용하지 않고 있습니다만, ESD 후 내시경을 빼기 전 위내 공기를 최대한 흡입하고 있습니다. 환자들의 시술 후 불편감이 훨씬 덜한 것 같습니다. [2015-11-29. 이준행]
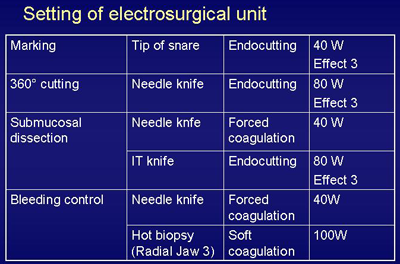
2004년 3월 28일 소화기내시경학회에 참석하였으며 gastric EMR 특히 submucosal dissection을 할 때 어떠한 setting으로 하는가에 대한 개인적인 질문을 여러번 받았습니다. 천기누설의 첫 내용은 이에 대한 답변입니다. Endoscopic mucosal resection을 함에 있어서 electrosurgical unit의 각 항목의 설정은 매우 중요하고도 어려운 문제입니다. 각 병원에서 사용하는 기구에 따라 달라지고 동일한 electrosurgical unit라 하더라도 knife나 snare의 종류에 따라서 달라지기도 합니다. 지속적으로 경험하면서 자기에게 가장 적합한 setting을 찾아보는 수 밖에 없습니다. 저는 ERBE ICC 200 을 사용하고 있으며 거의 대부분의 경우에 위에서 제시한 setting을 유지합니다. 다른 시술자들은 marking에서 Forced coagulation 25 W를 사용하는 경우가 많으며 argon plasma coagulation을 이용하여 marking을 할 수도 있습니다. Circumferential cutting (marginal cutting)전에 시행하는 precutting에서 needle knife를 쓰면서 coagulation mode로 setting을 하기도 하고 때로는 hot biopsy로 hole을 만들기도 합니다. Submucosal dissection 동안 Forced coagulation 50 W를 사용하는 시술자가 많으며 저도 최근 50 W를 쓰기도 합니다. 간혹 A.60을 선택하는 시술자도 있습니다만 예외적인 경우입니다. Hot biopsy forcep을 이용한 soft coagulation에서는 60-80 W를 사용하는 것이 일반적이지만, 소독한 hot biopsy forcep을 이용한 경우에는 100W가 보다 효과적인 것 같아서 저는 최근 80 W에서 100W 로 올려서 사용하고 있습니다. [2005. 4. 1.]
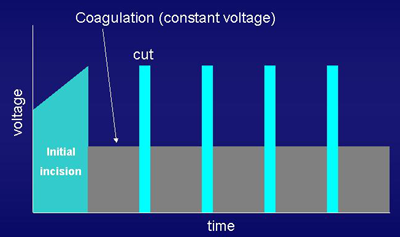
ICC-200의 Endocut current를 보여주는 그림입니다. Endocutting의 개념은 cutting current와 coagulation current를 자동적으로 alternation 시키는 것입니다. Cutting이 연속적으로 이루어지지 않고 사이사이 끊어지므로 control이 쉬워진다는 장점이 있으며 coagulation이 포함되므로 지혈효과가 우수하여 출혈이 적게 cutting을 할 수 있다는 점에서 매우 우수한 특성을 가진 mode 입니다. 그러나 cutting 속도가 다소 늦고 coagulation effect가 지나치게 많이 들어갈 수 있다는 단점이 지적되기도 합니다. 개량형인 VIO-300D에서는 Endocutting mode에서 cutting과 coagulation의 교차속도, 지속시간, 출력 등을 매우 섬세하기 조절할 수 있는 기능이 추가되었습니다. [2005. 2. 14.]

EMR에서 electrosurgical unit (ESU)의 성능은 매우 중요합니다. 빠르고 안전하게 시술을 마치기 위해서는 내시경과 부속기구 뿐만 아니라 ESU에 대한 매우 자세한 지식은 필수적입니다. 수년전부터 한국과 일본의 EMR 시술자들이 독일회사인 ERBE사 제품인 ICC-200, ICC-200D, VIO-300D 등을 선호하는 경향을 보이고 있습니다. 그 이유는 다른 회사의 ESU에 비하여 Endocutting과 Forced coagulation등의 다양한 current가 제공되므로 EMR 시술 도중 상황에 따라서 보다 적절한 전류의 선택을 할 수 있기 때문입니다. 조만간 Olympus에서도 Endocutting 과 유사한 기능을 가진 ESU를 시판할 예정인 것으로 알려져 있는데, 이 제품은 ERBE사에서 OEM 방식으로 납품한 것이라고도 합니다. 저도 최근 모든 EMR을 ERBE사의 Endocutting mode가 가능한 ESU를 이용하여 시술하고 있습니다.
문제는 학회에서의 강의와 문헌에서의 기술이 모두 ERBE사 제품의 ESU를 사용하는 것을 전제로 삼고 있기 때문에, 간혹 ERBE사의 ESU가 없으면 EMR, 특히 ESD를 시행할 수 없는 것으로 오해되는 경우가 있다는 점입니다. 물론 ERBE사의 Endocutting mode가 유용하기는 하지만 EMR의 필수적인 요소는 아닙니다. 근간에 제가 자주 듣게되는 질문의 하나가 "저희 병원에는 ERBE사의 ESU가 없는데 EMR을 하고 싶습니다. 가능하겠습니까? 할 수 있다면 어떤 setting으로 해야 좋을까요?"입니다. ESU의 setting은 하나로 정해진 것이 아닙니다. (1) 자신이 사용하는 ESU, 내시경, knife, snare 등의 종류, (2) 시술 도중 기구를 사용하는 시술자의 방식 (pressure 등), (3) reusable인지 single use인지 여부 (여러번 reuse하는 경우 약간 power를 올려주는 것이 좋다), (4) 병소의 특징 등에 따라서 달라지기 마련입니다. 저도 많은 종류의 ESU를 사용해보지 못했지만, Olympus PSD-10을 수 개월간 사용해본 경험이 있어서 당시 저희 병원에서 사용하던 setting을 공개합니다. 이러한 setting을 바탕으로 스스로 시술을 해 보면서 자신의 방식으로 조금씩 수정,보완해 가는 것이 최선의 방법이라고 생각합니다. [2005. 2. 11]
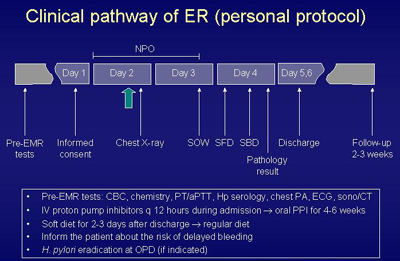
치료내시경에서 시술과 관련된 검사, 입원기간, 시술시간, 시술 직후의 검사, 입원시 투약, 퇴원의 결정, 퇴원시 투약, 추적관찰 방법 등은 시술자의 개인적인 경험에 의하여 결정되는 경우가 대부분입니다. superficial gastric neoplasm의 내시경적 치료에 있어서 제가 중요시하는 것은 환자의 안전과 정확한 결과의 판정입니다. 따라서 출혈의 위험성이 큰 기간 동안은 금식을 권하고 있으며 resected specimen의 pathology 결과가 나온 후 이를 바탕으로 환자와 의사가 향후 follow up 방침에 대하여 충분히 상의를 하고 퇴원하도록 하고 있습니다. 드물게 발생하는 일이지만 퇴원 후 집에서 melena나 hematemesis를 보이는 경우가 있으므로 주의를 요합니다. 재출혈의 위험이 높다고 판단되는 경우에는 입원기간을 다소 연장하는 것이 환자를 위험에 노출시키는 것 보다는 현명한 접근법이라고 믿습니다. Pathology 결과를 확인하지 않고 퇴원시키는 경우에는 외래에서 결과를 보게 되는데, 간혹 추가적인 수술이 필요한 경우가 발생하면 빠른 시술이 어려울 뿐만 아니라 환자와의 rapport가 깨지기 쉽습니다. 시술 후 일반적으로 PPI를 투여하고 있는데 투여기간에 대한 정설은 없습니다. 흔히 한달간 투약하는 것이 관례이지만 최근에는 submucosal dissection method를 이용하여 4-5 cm 이상의 광범위한 절제를 하는 경우도 적지 않으므로 환자에 따라 투약기간을 조절할 필요가 있습니다. [2004. 4.]

EMR의 방법에 따라 입원기간을 다소 연장시키거나 단축시킬 필요가 있습니다. 작은 hyperplastic polyp을 단순한 conventional snare resection을 하는 경우 입원시키지 않고 외래에서 시술하시는 선생님도 있습니다. 저는 inject and cut 방법으로 큰 hyperplastic polyp을 제거하는 경우에는 시술 다음날 퇴원시키고 있습니다. ESD는 다른 방법에 비하여 큰 병소도 en bloc으로 제거할 수 있다는 장점이 있지만 합병증의 위험이 큰 것도 사실입니다. 저는 ESD를 시행하는 환자에서도 EMR-P를 시행한 환자와 똑 같이 4-5박 정도의 schedule을 적용하고 있지만 의사에 따라서는 상당히 긴 입원기간을 권유하는 경우가 있습니다. 조기 퇴원의 경우 가정에서 지연출혈(delayed bleeding)을 하는 경우가 종종 있기 때문에 어떤 시점에서의 퇴원이 적절한지에 대한 consensus는 없습니다.
참고로 최근 문헌에 발표된 Shizuoka Cancer Center의 clinical pathway를 소개해 드리겠습니다. Shizuoka Cancer Center는 IT-knife를 이용한 ESD 방법을 처음으로 개발한 것으로 유명한 Dr. Ono 가 근무하고 있는 EMR 계에서는 매우 유명한 병원입니다. 저의 개인적인 protocol과 비교하여 보면 (1) 시술 2일전 입원시키고 있으며, (2) 시술 직후와 퇴원 직전에 내시경검사를 다시 시행하고, (3) 시술 후 약 7-8일 후에 퇴원시킨다는 점에서 차이를 보이고 있습니다. 이처럼 추적내시경 검사를 퇴원전에 2번이나 시행하고 (참고로 저는 퇴원전에 다시 내시경을 시행하지는 않고 있으며 시술 3-6개월 후에 첫 추적내시경을 시행하고 있습니다) 시술 일주일 후에 귀가를 시키면, 안전성은 다소 향상되겠으나 이로 인하여 환자에게 주어지는 고통은 상당할 것으로 생각됩니다. 현재 많은 병원에서 개복수술로 진행하는 subtotal gastrectomy의 입원기간이 10-11박 정도인 것을 생각하면 EMR 후 퇴원기간을 너무 늦게 잡는 관행은 다시 한번 고려할 필요가 있다고 생각됩니다. [2005. 2. 2.]

EMR, ESD를 시행할 때에 어떤 내시경을 사용하는지 질문하시는 분이 많습니다. 원칙적으로 어떤 내시경을 사용해도 무방하다고 생각합니다. 저는 최근 GIF-Q260을 주로 사용하고 있으며 과거에는 GIF-XQ240을 많이 사용하였습니다. Q type이 XQ type에 비하여 insertion tube의 outer diameter가 약 0.2 mm 정도 두껍습니다 (2.2% 차이). 이러한 두께의 차이는 매우 예민한 내시경의사 및 보조자도 알아차리기 어렵습니다. 환자가 모르는 것은 당연한 일입니다. 보다 중요한 차이는 Q type의 insertion tube가 약간 더 stiff하다는 점입니다. XQ type은 너무 flexible하여서 진단용으로는 좋으나 치료내시경용으로는 Q type보다 유용성이 떨어진다고 느끼고 있습니다. 약간 stiff한 내시경이 치료용으로는 더 좋습니다. Q type의 단점은 가격이 다소 비싸다는 점입니다.
위 그림의 제가 사용하는 두 종류의 내시경을 이용한 시술 장면을 capture한 것입니다. GIF-XQ240의 경우 화면이 정사각형으로 나오는 반면 GIF-Q260은 가로가 약간 긴 직사각형의 화면입니다. 처음에는 직사각형이 약간 부자연스럽게 느껴질 수 있으나 시술을 하면 할수록 좌우가 넓다는 점이 시야를 넓혀준다는 점에서 큰 장점으로 느껴집니다. 당연한 것인지 모르겠으나 240 series model에 비하여 260 series model의 화질이 더 좋으며, 같은 series에서는 XQ type의 화질에 비하여 Q type의 화질이 훨씬 우수합니다. H type은 더더욱 좋은 화질을 가지고 있으나 저는 아직 H type으로 EMR을 시행하고 있지는 않습니다 (너무 고가임). [2005. 4. 1]
 240 series와 260 series의 중요한 차이는 bending section의 길이가 다르다는 점입니다. 260 series는 bending part의 길이가 짧아서 duodenal bulb안에서 retroflection이 가능합니다. 최근의 새로운 모델은 더욱 다양한 특성을 가지고 있습니다. 이러한 특성(짧은 bending section)을 이용하여 pyloric ring에 걸쳐있는 종양에 대한 내시경 절제술을 시행할 수 있습니다. 비록 retroflection이 되더라도 활동 반경이 좁아서 pyloric ring에서 duodenal bulb에 걸쳐 있는 병소에 대한 효과적인 시술은 어렵습니다. [2005-4-1. 이준행]
240 series와 260 series의 중요한 차이는 bending section의 길이가 다르다는 점입니다. 260 series는 bending part의 길이가 짧아서 duodenal bulb안에서 retroflection이 가능합니다. 최근의 새로운 모델은 더욱 다양한 특성을 가지고 있습니다. 이러한 특성(짧은 bending section)을 이용하여 pyloric ring에 걸쳐있는 종양에 대한 내시경 절제술을 시행할 수 있습니다. 비록 retroflection이 되더라도 활동 반경이 좁아서 pyloric ring에서 duodenal bulb에 걸쳐 있는 병소에 대한 효과적인 시술은 어렵습니다. [2005-4-1. 이준행]
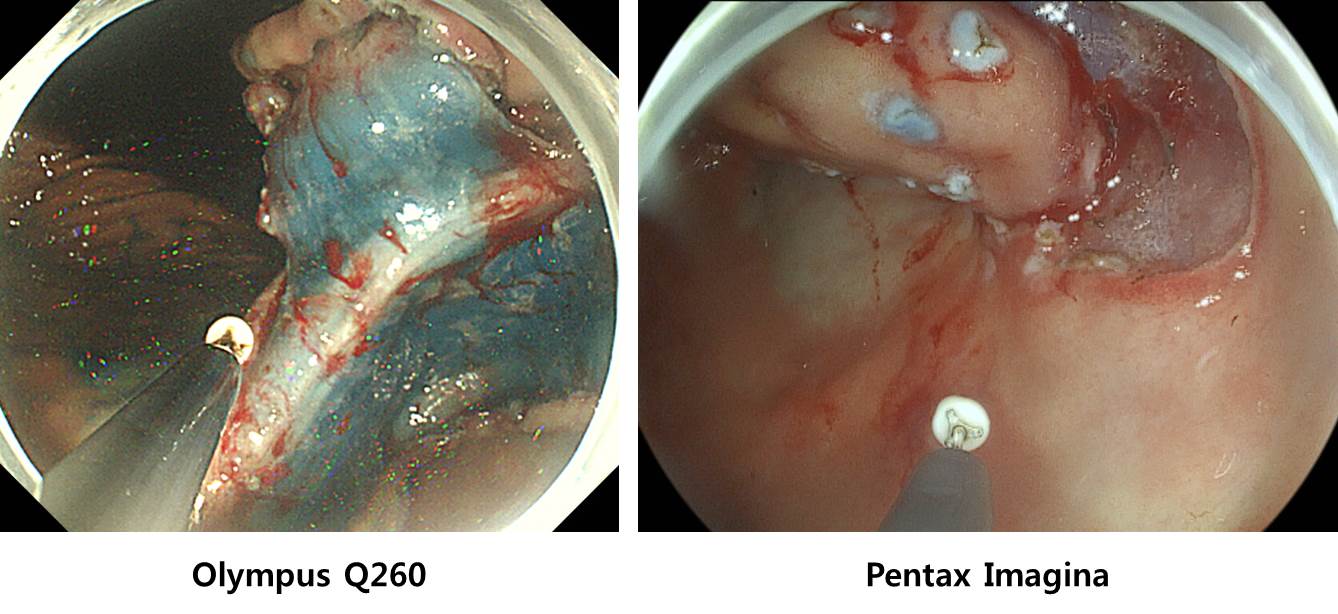 요즘 ESD에는 Pentax Imagina 내시경을 사용하고 있습니다. 화면에서 working channel의 위치(ESD knife가 나오는 곳)가 조금 달라 처음 한 case는 약간 어색했는데, 두번째 case 부터는 매우 자연스러워졌습니다. 몇 도 안 되는 차이인지라 금방 적응할 수 있다고 생각됩니다. [2019-4-10. 이준행]
요즘 ESD에는 Pentax Imagina 내시경을 사용하고 있습니다. 화면에서 working channel의 위치(ESD knife가 나오는 곳)가 조금 달라 처음 한 case는 약간 어색했는데, 두번째 case 부터는 매우 자연스러워졌습니다. 몇 도 안 되는 차이인지라 금방 적응할 수 있다고 생각됩니다. [2019-4-10. 이준행]
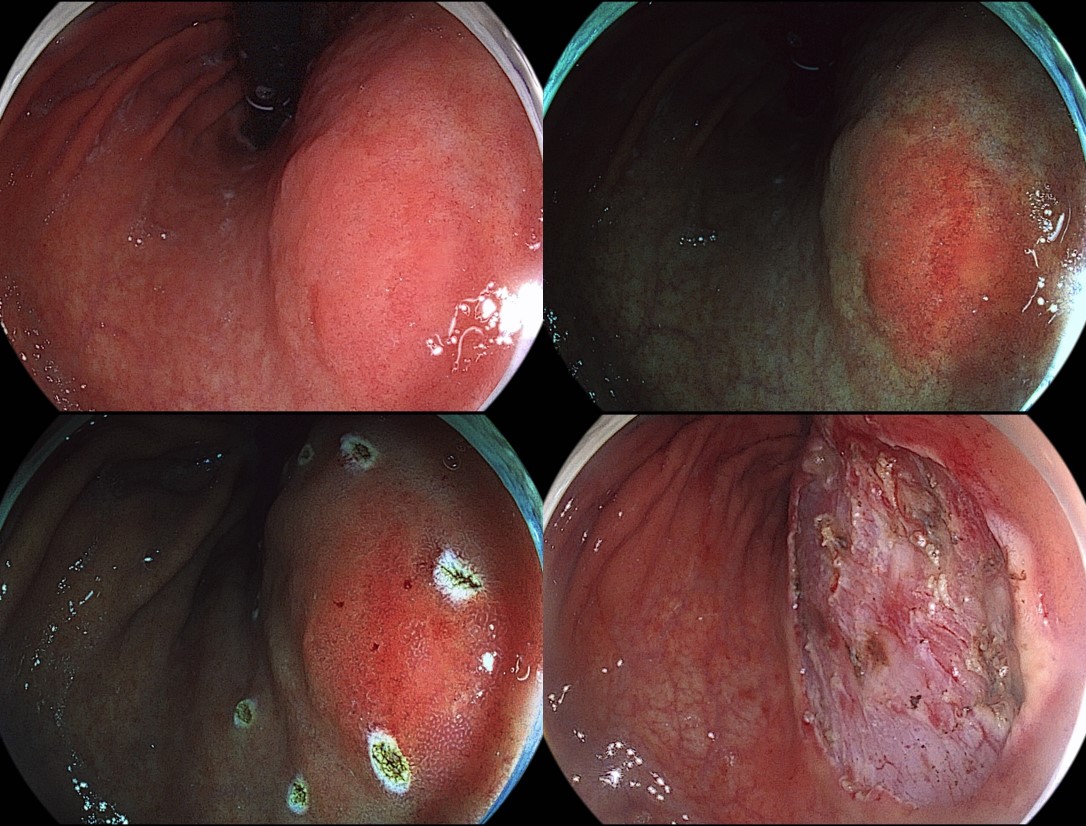 2020년 4월 새로운 내시경 system을 도입하여 ESD를 하고 있습니다. 색감과 focus와 손맛이 조금 다르지만 적응하는데는 전혀 어려움이 없었습니다.
2020년 4월 새로운 내시경 system을 도입하여 ESD를 하고 있습니다. 색감과 focus와 손맛이 조금 다르지만 적응하는데는 전혀 어려움이 없었습니다.
ESD: Tubular adenoma with low grade dysplasia
1. Location : mid-body, lesser curvature
2. Gross type : flat
3. Size of adenoma : (1) longest diameter, 20 mm (2) vertical diameter, 13 mm
4. Resection margin : negative resection margins(N)
 직장 ESD를 위하여 위내시경을 사용하는 경우가 있습니다. 가늘고 각도가 잘 나오기 때문입니다. 최근 Olympus에서는 PCF-H290TL/I (catalog)이라는 신형 대장내시경을 발매하였습니다. 이름만 보면 소아용 대장내시경(P로 시작)같은데, 기능은 완전히 성인 직장/대장 ESD 전용 내시경입니다. 주된 특징은 (1) 가늘다, (2) angulation이 잘 나온다, (3) water jet 기능이 있다, (4) variable stiffness 기능이 있다, (5) colonoscopy 용 balloon overtube를 사용할 수 있다 등입니다. 한 마디로 이제는 대장 ESD를 위하여 위내시경을 사용할 필요가 없다는 것입니다. [2019-11-4. 이준행]
직장 ESD를 위하여 위내시경을 사용하는 경우가 있습니다. 가늘고 각도가 잘 나오기 때문입니다. 최근 Olympus에서는 PCF-H290TL/I (catalog)이라는 신형 대장내시경을 발매하였습니다. 이름만 보면 소아용 대장내시경(P로 시작)같은데, 기능은 완전히 성인 직장/대장 ESD 전용 내시경입니다. 주된 특징은 (1) 가늘다, (2) angulation이 잘 나온다, (3) water jet 기능이 있다, (4) variable stiffness 기능이 있다, (5) colonoscopy 용 balloon overtube를 사용할 수 있다 등입니다. 한 마디로 이제는 대장 ESD를 위하여 위내시경을 사용할 필요가 없다는 것입니다. [2019-11-4. 이준행]
2025년 O사에서 새로운 내시경을 보급하기 시작하였습니다. GIF-H290T입니다. 290 시리즈에 working channel 내경 2.8mm 밖에 없어서 치료내시경이 어려웠는데 GIF-H290T은 내경이 3.2mm 이므로 260J처럼 catheter를 넣은 상태에서 공기 흡입이 가능하므로 치료내시경이 훨씬 쉬워졌습니다. RDI라는 mode가 있어서 active bleeding spot이 더 잘 관찰되는 특장점도 있습니다.
 Fundus는 ESD가 어려운 부위입니다. 그러나 fundus도 넓습니다. 위치에 따라 다릅니다. 내시경 치료가 가능한 부위도 넓습니다.
Fundus는 ESD가 어려운 부위입니다. 그러나 fundus도 넓습니다. 위치에 따라 다릅니다. 내시경 치료가 가능한 부위도 넓습니다.
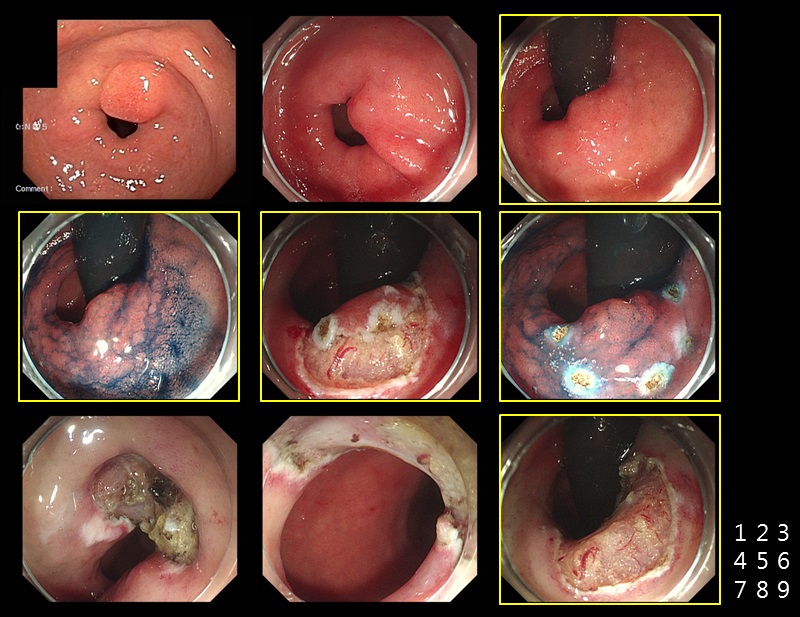 Pyloric ring 종양은 내시경 치료가 어렵습니다. 특히 종양의 일부는 위에, 일부는 십이지장에 위치하는 경우는 더욱 그러합니다. 십이지장 구부에서 내시경을 retroflection 시켜 부분 ESD를 시행하고, 이어서 위에서 나머지 부분을 시술하는 방식을 사용할 수 있습니다. 십이지장 구부가 넓지 않아서 retroflection이 잘 되지 않는 환자에서는 적용할 수 없는 방법입니다. 증례는 날문의 고도선종이었으며 일부는 십이지장으로 extension을 보이고 있었습니다. 노란색 box로 표시한 그림은 십이지장에서 retroflection하여 관찰하고 시술하는 장면입니다. 종양은 en bloc resection을 할 수 있었고, 이 과정에서 pyloric ring의 circumference 40% 정도가 절제되었습니다. [2017-7-19. 이준행]
Pyloric ring 종양은 내시경 치료가 어렵습니다. 특히 종양의 일부는 위에, 일부는 십이지장에 위치하는 경우는 더욱 그러합니다. 십이지장 구부에서 내시경을 retroflection 시켜 부분 ESD를 시행하고, 이어서 위에서 나머지 부분을 시술하는 방식을 사용할 수 있습니다. 십이지장 구부가 넓지 않아서 retroflection이 잘 되지 않는 환자에서는 적용할 수 없는 방법입니다. 증례는 날문의 고도선종이었으며 일부는 십이지장으로 extension을 보이고 있었습니다. 노란색 box로 표시한 그림은 십이지장에서 retroflection하여 관찰하고 시술하는 장면입니다. 종양은 en bloc resection을 할 수 있었고, 이 과정에서 pyloric ring의 circumference 40% 정도가 절제되었습니다. [2017-7-19. 이준행]
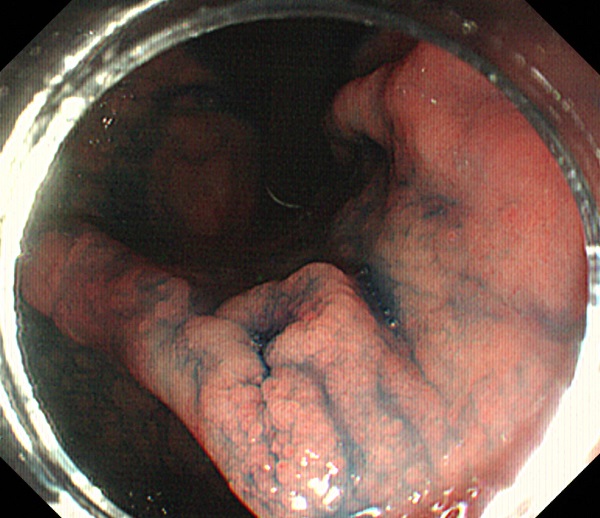 위암이나 위선종의 내시경치료에 transparent hood는 필수적입니다. 과거에는 일본 O사의 투명캡을 사용했습니다. 최근 국내에서 개발된 제품으로 변경하여 사용하고 있습니다. 대구에 본거지를 둔 F사 제품입니다 (FM-EC000412.4mm - 외경이 12.4mm인 제품입니다). 점차적으로 국산 도구 사용률을 높이려고 계획하고 있습니다. [2017-6-7]
위암이나 위선종의 내시경치료에 transparent hood는 필수적입니다. 과거에는 일본 O사의 투명캡을 사용했습니다. 최근 국내에서 개발된 제품으로 변경하여 사용하고 있습니다. 대구에 본거지를 둔 F사 제품입니다 (FM-EC000412.4mm - 외경이 12.4mm인 제품입니다). 점차적으로 국산 도구 사용률을 높이려고 계획하고 있습니다. [2017-6-7]
[Fujifilm Flush knife BT]
여러 회사에서 다양한 ESD knife를 만들고 있습니다. 최근 병원에 도입한 모델은 Fujifilm 사의 Flush knife입니다. [2022-5-7]
Flush knife. Needle type knife를 Fujifilm에서는 두 가지로 만들고 있습니다. 끝에 ball이 있는 것과 없는 것입니다. (브로셔) [2017-6-26]
Flush knife BT (브로셔) [2017-6-26]
우연히 발견된 경계가 매우 불분명한 작은 함몰형 조기위암을 ball-type Flush knife 2mm를 이용하여 ESD로 치료하였습니다.
이렇게 경미한 slightly depressed lesion을 발견하고 조직검사로 암을 진단한다는 것은 정말 대단한 일입니다. 지역의 내과의원이었는데 정말 대단한 일을 하셨습니다. 의뢰서 내용입니다. "내시경 상 전정부 원위 소만 미세 점막변형 EGC 2B about 5mm"
2023년 4월 Boston 사의 ORISE knife도 사용하고 있습니다.
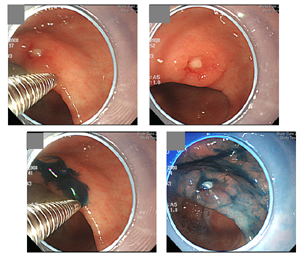
EMR/ESD가 기술적으로 mature해지기 전까지는 어떻게하면 안전하게 원하는 부위를 en bloc으로 자를 것이지가 초미의 관심사였습니다. 그러나 EMR/ESD가 기술적으로 mature해진 현 상태에서는 어떤 병소를 얼마만큼 자를 것인지가 다시 중요해졌다고 생각합니다. Technique이 발전하면서 광란의 시기- indication을 고려하지 않고 자를 수 있는 것은 다 자른다는 것이 유행인 때도 있었습니다- 가 지나가고 다시 한번 어떠한 병소가 EMR/ESD의 치료대상으로 적당한지를 진지하게 검토해야 하는 시대가 되었다는 말입니다. 이를 위하여 병소의 경계를 정확하게 결정하는 것이 매우 중요합니다. Magnifying endoscope라는 것이 있지만 필자는 아직까지 확대내시경이 EMR/ESD 환자의 치료에 도움이 된다고 생각하지 않습니다. 여전히 가장 중요한 tool은 indigocarmine을 이용한 chromoendoscopy입니다. 과거에는 Olympus사의 spraying catheter를 이용하여 넓은 부위에 골고루 색소를 살포하는 방법을 썼습니다. 그러나 최근에는 injection needle을 이용하여 needle을 내지 않은 상태에서 천천히 색소를 중력을 이용하여 흘리는 방법을 사용하고 있습니다. 이 방법은 몇 가지 장점이 있습니다. (1) 사용되는 색소의 양이 작습니다. (2) 색소가 뿌려지지 않고 흘러가는 것이므로 강한 색소살포에 의하여 병소에서 출혈이 되는 일이 없습니다. (3) Spraying catheter를 사용하지 않기 때문에 EMR/ESD에서 사용되는 도구의 수가 줄어들게 됩니다. (4) Marking을 하지 않고 시술을 할 경우에는 injection needle을 이용하여 색소를 뿌려 관찰한 직후에 submucosal injection을 바로 할 수 있으므로 시간이 절약됩니다. EMR/ESD는 매우 복잡한 시술입니다. 시술 도중에 사용되는 소도구를 하나라도 줄이려는 노력은 시술에 따른 시간과 비용을 줄여줄 뿐만 아니라 감염의 위험성도 감소시켜주기 때문에 항상 도움이 됩니다. [2008.6.15.]
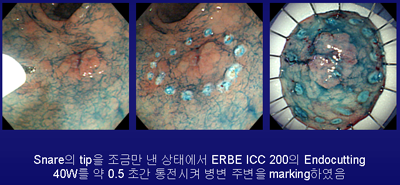
병변 주변에 marking을 하는 방법은 매우 다양합니다. Needle knife를 이용하여 coagulation current를 이용하는 것이 일반적이지만, 저는 최근 snare의 tip을 조금만 낸 상태에서 Endocutting current를 매우 짧게 통과시키는 방법을 이용하고 있습니다. 기존의 방법에 비하여 marking이 보다 선명하고 tissue의 distruction이 적다는 인상을 받았기 때문입니다. 이 방법은 Flex knife를 이용한 ESD에서 이용되는 방법과 유사하다고 생각하시면 됩니다. [2005. 2. 1.]
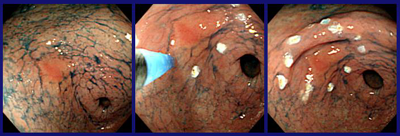
Argon plasma coagulation을 이용하여 marking을 할 수도 있습니다. 병소가 약간 oblique 한 곳에 위치하더라도 빠른 시간에 선명한 marking을 남긴다는 장점이 있습니다. 그러나 다른 방법에 비하여 tissue destruction은 더 심한 편입니다. 또한 electrosurgical unit (ESU) 이외에 APC를 위한 장비가 필요하므로 복잡하고 비용이 많이 소요됩니다. 간단한 방법을 좋아하는 시술자는 ESD의 모든 과정을 needle knife 하나만을 - 아직 국내에 수입되어 있지 않지만 일본에서는 Flex knife 하나만을 - 이용하기도 합니다. 저도 간단한 방법을 좋아하는 편입니다. 반대로 현란한 techinique을 즐기는 시술자는 한 환자의 시술에서 여러 종류의 많은 도구를 사용합니다. 그러나 한 환자의 시술에 고가의 일회용 장비를 여러개 사용하는 것이 현실적으로 쉽지는 않습니다. [2005. 4. 14.]
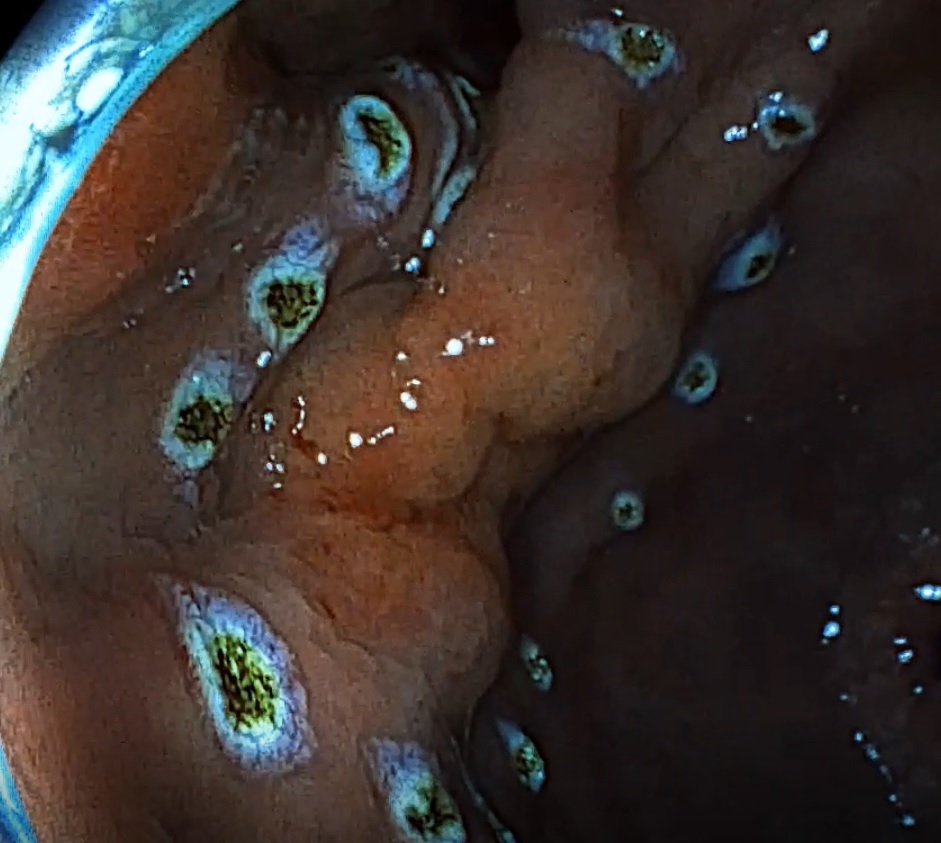
 과거 내시경에 비하여 최근의 내시경은 focus가 가깝게 설정되어 있습니다. Pentax Imagina 내시경이 특히 그러합니다. ESD 전 자연광 및 i-Scan close up view를 이용하여 병소의 margin을 평가할 수 있으며 ingidocarmine spry step을 생략할 수 있어서 편리합니다. [2020.4.30]
과거 내시경에 비하여 최근의 내시경은 focus가 가깝게 설정되어 있습니다. Pentax Imagina 내시경이 특히 그러합니다. ESD 전 자연광 및 i-Scan close up view를 이용하여 병소의 margin을 평가할 수 있으며 ingidocarmine spry step을 생략할 수 있어서 편리합니다. [2020.4.30]
 Submucosal injection을 할때 indigocarmine을 적당히 섞어주면 injection 된 부위가 파랗게 변하므로 크게 도움이 됩니다. 저는 normal saline과 epinephrine 및 indigocarcmine을 위의 처방대로 사용하고 있습니다. Indigocarmine은 제가 근무하는 병원의 약제부에서 만든 0.4% 용액을 이용하고 있습니다. (2004-3-2)
Submucosal injection을 할때 indigocarmine을 적당히 섞어주면 injection 된 부위가 파랗게 변하므로 크게 도움이 됩니다. 저는 normal saline과 epinephrine 및 indigocarcmine을 위의 처방대로 사용하고 있습니다. Indigocarmine은 제가 근무하는 병원의 약제부에서 만든 0.4% 용액을 이용하고 있습니다. (2004-3-2)
2004년 초, 동경대학의 Yahagi 교수팀이 고농도 hyaluronic acid의 EMR에서의 유용성에 대한 좋은 자료를 유럽내시경학회지에 발표하였습니다 (Endoscopy 2004;36:579-583). 그러나 2004년 가을, hyaluronic acid가 wound site에서 tumor cell proliferation을 촉진시킬 수 있다는 매우 impressive한 동물실험 결과가 미국내시경학회지에 발표되어 submucosal injection solution의 안전성에 대한 의문이 제기되고 있습니다 (Gastrointest Endosc 2004;60:539-543). 아무리 사소한 것이라고 하더라도 사람의 몸에 사용하는 것은 효과와 안전성에 대한 검토를 충분히 시행한 후 이용하는 것이 좋을 것으로 생각됩니다 (2005-2-2)
위치가 어렵거나 다른 이유로 lifting이 오래 지속되어야 할 경우에는 10% glycerin 500 ml + epinephrine 5 ampules + indigocarmine (40mg/5ml) 0.1-5ml을 쓰기도 합니다. 다만 이런 solution을 쓰게 되면 injector needle을 매우 세게 눌러야 합니다 (2020-2-13).
[2023-6-21. 김은란 교수님께서 알려주신 정보] 점막하주입용액으로 Sod. hyaluronate가 원내에서 사용가능하게 되었습니다. Sod. hyaluronate (20 ml)와 thrombin이 하나의 set로 되어 있는 제품으로, Sodium hyaluronate 를 원하시는 점도에 따라 NS에 mix하여 점막하주입용액으로 사용하실 수 있고, thrombin은 thrombin 용해제와 섞어서 ESD 시행 후 절제면에 working channel을 통해 도포해 주시면 도움이 될 것 같습니다. 내시경실에 미리 배치해 두기는 어려워, 사용 예정이실 경우 내시경실에 미리 준비를 요청해 주시면 좋을 것 같습니다. 비용은 비급여로 89,000원 입니다.
 위는 주머니처럼 생긴 기관이므로 내시경으로 들여다 보았을 때 oblique한 위치에 병소가 발견되는 예가 많습니다. 이 경우 병소의 4 방향에 동시에 submucosal injection을 시행하면 내시경에서 먼 쪽의 circumferential cutting이 어려워지는 수가 있습니다. 이를 방지하기 위하여 cutting이 어려울 것으로 생각되는 먼 부위에 대하여 먼저 submucosal injection을 시행한 후 이 부위에 대한 cutting을 마치고, 이어서 나머지 부위에 대한 submucosal injection을 시행하면 의외로 쉬울 수 있습니다. 저는 이러한 방법을 partial submucosal injection method라 부르고 있는데 아주 자주 사용하는 편입니다. 약간 시간이 더 걸린다는 단점이 있지만 훨씬 안전하고 효과적이라는 개인적인 인상을 가지고 있습니다. EMR은 묘기대행진이 아닐 것입니다. 믿거나 말거나는 더더욱 아닙니다. 얼마나 빨리 시술을 마치는가에 대하여, 혹은 얼마나 크게 병소를 절제하였는가에 대하여 자랑을 하는 것은 겸손한 의사의 태도는 아닐 것입니다. (2005-2-3)
위는 주머니처럼 생긴 기관이므로 내시경으로 들여다 보았을 때 oblique한 위치에 병소가 발견되는 예가 많습니다. 이 경우 병소의 4 방향에 동시에 submucosal injection을 시행하면 내시경에서 먼 쪽의 circumferential cutting이 어려워지는 수가 있습니다. 이를 방지하기 위하여 cutting이 어려울 것으로 생각되는 먼 부위에 대하여 먼저 submucosal injection을 시행한 후 이 부위에 대한 cutting을 마치고, 이어서 나머지 부위에 대한 submucosal injection을 시행하면 의외로 쉬울 수 있습니다. 저는 이러한 방법을 partial submucosal injection method라 부르고 있는데 아주 자주 사용하는 편입니다. 약간 시간이 더 걸린다는 단점이 있지만 훨씬 안전하고 효과적이라는 개인적인 인상을 가지고 있습니다. EMR은 묘기대행진이 아닐 것입니다. 믿거나 말거나는 더더욱 아닙니다. 얼마나 빨리 시술을 마치는가에 대하여, 혹은 얼마나 크게 병소를 절제하였는가에 대하여 자랑을 하는 것은 겸손한 의사의 태도는 아닐 것입니다. (2005-2-3)
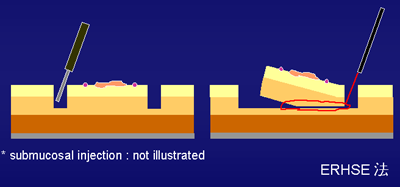 EMR-P 법의 모식도입니다. 병변 주위를 자른 후 snare로 resection을 하는 방법인데 시간은 무척 절약이 되지만 큰 병소를 en bloc resection하는데 제한점이 있으며 간혹 병소의 중간부분만 남기고 주변부만 도넛 모양으로 잘리는 황당한 경우가 발생하기도 합니다. 최근에는 ESD와 EMR-P를 혼합하여 partial submucosal dissection후 snare resection을 함으로써 큰 병소를 안전하게 en bloc resection 하면서도 시간을 절약하는 방법을 사용하는 시술자가 많습니다. (2005-2-1)
EMR-P 법의 모식도입니다. 병변 주위를 자른 후 snare로 resection을 하는 방법인데 시간은 무척 절약이 되지만 큰 병소를 en bloc resection하는데 제한점이 있으며 간혹 병소의 중간부분만 남기고 주변부만 도넛 모양으로 잘리는 황당한 경우가 발생하기도 합니다. 최근에는 ESD와 EMR-P를 혼합하여 partial submucosal dissection후 snare resection을 함으로써 큰 병소를 안전하게 en bloc resection 하면서도 시간을 절약하는 방법을 사용하는 시술자가 많습니다. (2005-2-1)
 외래를 보던 중 2004년 시술 했던 환자를 만났습니다. EMR-P with partial submucosal dissection을 시행했더군요. ESD가 쉽지 않았던 시절이었습니다. ESD를 배우겠다고 일본을 왔다갔다 했던 생각이 납니다 (이준행의 2004년 일본 ESD 현장 탐방기). 당시에는 circumferential precutting 후 snare resection하는 방법을 주로 사용하였습니다. Snare로 en bloc resection이 어렵다고 생각되면 needle knife로 조심스럽게 partial submucosal dissection을 하였는데 그 과정에서 종종 perforation이 발생하였습니다. 이제는 IT-knife와 Dual knife 등이 있어서 훨씬 안전하게 훨씬 완벽하게 시술할 수 있게 되었습니다. 현재의 문제는 1.5cm가 되지 않는 선종은 안전하고 효과적인 ESD 방법을 적용할 수 없다는 감독기관의 규정입니다. 좋은 방법이 있는데 후진 방법을 쓰라고 강요하니 참 안타까운 일입니다. 환자 중심의 의료 체계를 기대하는 것은 저의 헛된 꿈일까요? (2019-4-16)
외래를 보던 중 2004년 시술 했던 환자를 만났습니다. EMR-P with partial submucosal dissection을 시행했더군요. ESD가 쉽지 않았던 시절이었습니다. ESD를 배우겠다고 일본을 왔다갔다 했던 생각이 납니다 (이준행의 2004년 일본 ESD 현장 탐방기). 당시에는 circumferential precutting 후 snare resection하는 방법을 주로 사용하였습니다. Snare로 en bloc resection이 어렵다고 생각되면 needle knife로 조심스럽게 partial submucosal dissection을 하였는데 그 과정에서 종종 perforation이 발생하였습니다. 이제는 IT-knife와 Dual knife 등이 있어서 훨씬 안전하게 훨씬 완벽하게 시술할 수 있게 되었습니다. 현재의 문제는 1.5cm가 되지 않는 선종은 안전하고 효과적인 ESD 방법을 적용할 수 없다는 감독기관의 규정입니다. 좋은 방법이 있는데 후진 방법을 쓰라고 강요하니 참 안타까운 일입니다. 환자 중심의 의료 체계를 기대하는 것은 저의 헛된 꿈일까요? (2019-4-16)
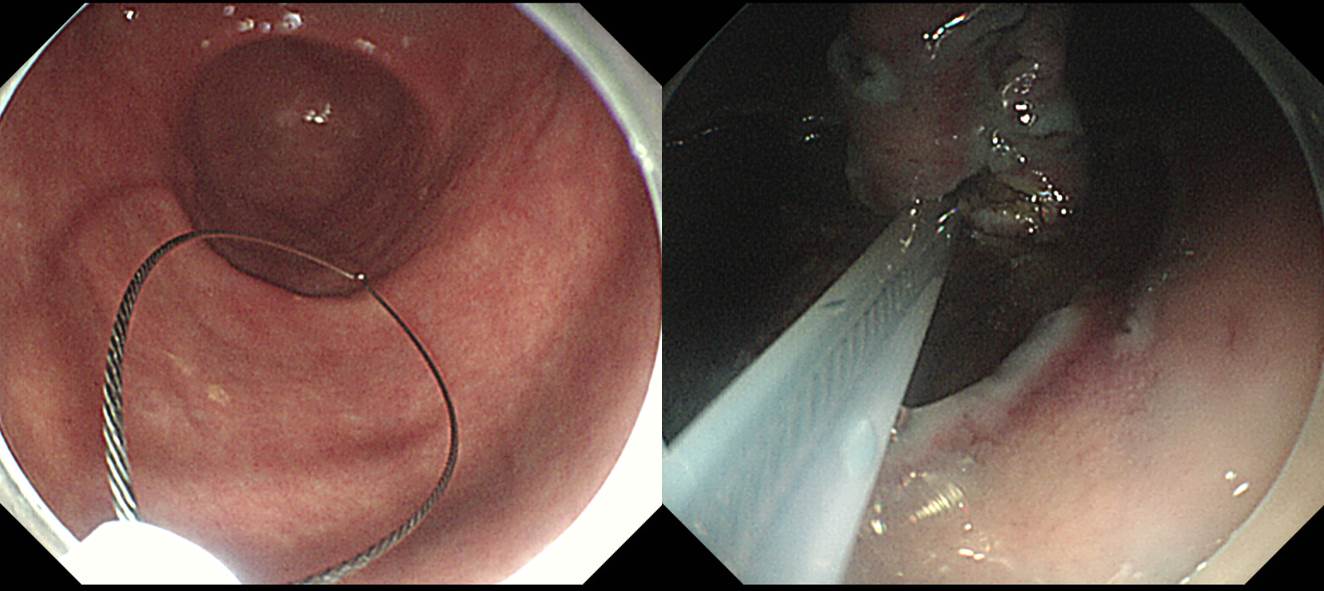 EMR polypectomy, EMR-P (precutting), snare resection after partial ESD 후 snare를 이용하여 절제술을 하게 됩니다. 과거에는 전부 일본 O사 제품을 사용하였는데 최근에는 국산의 품질이 좋아져서 Finemedix 제품을 쓰기 시작하였습니다. (2018-4-5)
EMR polypectomy, EMR-P (precutting), snare resection after partial ESD 후 snare를 이용하여 절제술을 하게 됩니다. 과거에는 전부 일본 O사 제품을 사용하였는데 최근에는 국산의 품질이 좋아져서 Finemedix 제품을 쓰기 시작하였습니다. (2018-4-5)
 앞서 언급한 partial submucosal dissetion의 예 입니다. ESD에서 마지막 조금 남은 submucosal tissue를 절제하는 것은 항상 어려운 일인데 이와 같이 조금 남은 상태에서 snare resection을 하면 상당한 시간을 절약할 수 있습니다. (2005-2-1)
앞서 언급한 partial submucosal dissetion의 예 입니다. ESD에서 마지막 조금 남은 submucosal tissue를 절제하는 것은 항상 어려운 일인데 이와 같이 조금 남은 상태에서 snare resection을 하면 상당한 시간을 절약할 수 있습니다. (2005-2-1)
 일본에서 ESD 술기를 발전시키는 초기에 Yahagi 선생님이 Flex-knife를 개발한 바 있습니다. Snare tip을 이용하여 ESD를 하던 경험을 바탕으로 ESD 전용 knife를 만들었던 것입니다. 현재는 Dual knife에 밀려서 거의 사용되지는 않지만 snare tip으로 ESD를 할 수 있다는 사실은 아직도 유효합니다. 특히 snare를 이용한 EMR polypectomy를 하면서 동시에 ESD를 할 경우에는 snare를 사용한 후 연이어 snare tip을 이용한 ESD를 하는 것이 가능합니다. Snare는 snare 대로 사용하도 Dual knife 같은 ESD 전용 knife도 함께 사용하는 것 보다는 snare 하나로 EMR도 하고 ESD도 할 수 있으니 경제적입니다. 그런데 주의해야 할 점이 있습니다. Snare tip을 이용한 ESD는 우리나라에서 인정되지 않고 있습니다. 전용 knife만을 사용하여 시술한 경우만 ESD로 인정할 수 있다니 답답할 따름입니다. (2019-11-1)
일본에서 ESD 술기를 발전시키는 초기에 Yahagi 선생님이 Flex-knife를 개발한 바 있습니다. Snare tip을 이용하여 ESD를 하던 경험을 바탕으로 ESD 전용 knife를 만들었던 것입니다. 현재는 Dual knife에 밀려서 거의 사용되지는 않지만 snare tip으로 ESD를 할 수 있다는 사실은 아직도 유효합니다. 특히 snare를 이용한 EMR polypectomy를 하면서 동시에 ESD를 할 경우에는 snare를 사용한 후 연이어 snare tip을 이용한 ESD를 하는 것이 가능합니다. Snare는 snare 대로 사용하도 Dual knife 같은 ESD 전용 knife도 함께 사용하는 것 보다는 snare 하나로 EMR도 하고 ESD도 할 수 있으니 경제적입니다. 그런데 주의해야 할 점이 있습니다. Snare tip을 이용한 ESD는 우리나라에서 인정되지 않고 있습니다. 전용 knife만을 사용하여 시술한 경우만 ESD로 인정할 수 있다니 답답할 따름입니다. (2019-11-1)
 제가 가장 흔하게 사용하는 방법의 하나인 ESD의 모식도입니다. ESD는 여러가지 도구를 이용하여 시행할 수 있습니다. 일본에서는 IT knife를 이용한 방법이 가장 많이 사용되며, Flex knife나 Hook knife를 사용하는 경우도 있습니다. Double ballon enteroscopy로 유명한 지치대학의 Yamamoto는 IT knfe, Flex knife, Hook knife를 사용하지 않고 narrow tipped hood를 내시경 끝에 작착한 후 needle knife를 이용하여 직접 submucosal dissection을 하고 있습니다. 각 방법마다 장점은 있지만 일본에서 가장 널리 사용되는 방법은 동경암센터에서 주로 이용하고 있는 IT knife법입니다. 그러나 일부 시술자들은 Flex knife법이 시간은 조금 더 걸리지만 배우기 쉽고 안전한 방법이라고 하여 많이 사용하고 있습니다. 2005년 1월 현재 우리나라에는 IT knife, Flex knife, Hook knife, narrow tipped hood가 모두 정식으로 수입되어 있지 않습니다. 따라서 저는 Yamamoto 방법을 변형하여 MTW사의 needle knife를 이용한 direct cutting에 의한 submucosal dissection method를 주로 사용하고 있습니다. 처음에는 perforation의 위험이 있으나 익숙해 지면 Flex knife법과 거의 유사한 technique를 구사할 수 있습니다. 향후 Flex knife가 정식으로 수입되면 이를 사용해 볼 계획으로 있습니다. (2005-2-1)
제가 가장 흔하게 사용하는 방법의 하나인 ESD의 모식도입니다. ESD는 여러가지 도구를 이용하여 시행할 수 있습니다. 일본에서는 IT knife를 이용한 방법이 가장 많이 사용되며, Flex knife나 Hook knife를 사용하는 경우도 있습니다. Double ballon enteroscopy로 유명한 지치대학의 Yamamoto는 IT knfe, Flex knife, Hook knife를 사용하지 않고 narrow tipped hood를 내시경 끝에 작착한 후 needle knife를 이용하여 직접 submucosal dissection을 하고 있습니다. 각 방법마다 장점은 있지만 일본에서 가장 널리 사용되는 방법은 동경암센터에서 주로 이용하고 있는 IT knife법입니다. 그러나 일부 시술자들은 Flex knife법이 시간은 조금 더 걸리지만 배우기 쉽고 안전한 방법이라고 하여 많이 사용하고 있습니다. 2005년 1월 현재 우리나라에는 IT knife, Flex knife, Hook knife, narrow tipped hood가 모두 정식으로 수입되어 있지 않습니다. 따라서 저는 Yamamoto 방법을 변형하여 MTW사의 needle knife를 이용한 direct cutting에 의한 submucosal dissection method를 주로 사용하고 있습니다. 처음에는 perforation의 위험이 있으나 익숙해 지면 Flex knife법과 거의 유사한 technique를 구사할 수 있습니다. 향후 Flex knife가 정식으로 수입되면 이를 사용해 볼 계획으로 있습니다. (2005-2-1)
Flexknife가 정식으로 수입되어 한 동안 사용하였습니다. 이후로는 Dual knife로 대체하였습니다. 보다 안정적인 시술을 할 수 있기 때문입니다. (2018-8-29)
국산 ESD knife의 품질이 날로 좋아지고 있습니다. 최근에는 Finemedix 사의 ClearCut Knife들을 사용하기 시작하였습니다. (2018-12-20)
 Finemedix J knife를 이용한 ESD (2018, F/62)
Finemedix J knife를 이용한 ESD (2018, F/62)
Finemedix ClearCut 계열의 J knife (FM-EK0005-1.5(1820)) 입니다. I knife와 동일한데 water jet function이 가능한 모델입니다. 전용 펌프를 가지고 있지 않아서 우선 water jet 기능은 사용하지 않고 needle type knife와 비슷하게 시술하였습니다. 기존의 일본 제품과 크게 차이가 없어서 적응기간 없이 바로 사용할 수 있었습니다. Water jet 기능을 사용하면 더욱 좋을 것 같습니다. (2018-12-20)
2022-3-20 내시경학회에서 Finemedix ESD knife 새 카타로그를 보았습니다.
 Gastric ESD를 할 수 있는 도구는 매우 많습니다. 저는 IT knife로 배웠고, Flex knife와 IT-2로 바꾸었고, 수 년 전부터는 Dual knife를 주로 사용하고 있습니다. ESD를 할 때 한 명에서 한 개의 knife만 사용하라는 정부의 방침에 기인한 바 큽니다. 일회용 도구를 하나만 쓰라고 하니 IT-2 knife에서 Dual knife로 바꿨던 것입니다. 간혹 Dual knife와 IT-2 knife를 모두 써야 하는 경우도 있습니다. 위치나 fibrosis 때문입니다. 국내 ESD knife의 품질이 매우 좋아졌습니다. Finemedix에서 나온 ClearCut knife H type은 IT knife와 Dual knife의 장점을 모은 혁신적인 제품입니다. 검토 중인데요... 여차하면 저의 主 무기를 국산 H type knife로 바꿀까 고민 중입니다. (2019-1-2)
Gastric ESD를 할 수 있는 도구는 매우 많습니다. 저는 IT knife로 배웠고, Flex knife와 IT-2로 바꾸었고, 수 년 전부터는 Dual knife를 주로 사용하고 있습니다. ESD를 할 때 한 명에서 한 개의 knife만 사용하라는 정부의 방침에 기인한 바 큽니다. 일회용 도구를 하나만 쓰라고 하니 IT-2 knife에서 Dual knife로 바꿨던 것입니다. 간혹 Dual knife와 IT-2 knife를 모두 써야 하는 경우도 있습니다. 위치나 fibrosis 때문입니다. 국내 ESD knife의 품질이 매우 좋아졌습니다. Finemedix에서 나온 ClearCut knife H type은 IT knife와 Dual knife의 장점을 모은 혁신적인 제품입니다. 검토 중인데요... 여차하면 저의 主 무기를 국산 H type knife로 바꿀까 고민 중입니다. (2019-1-2)
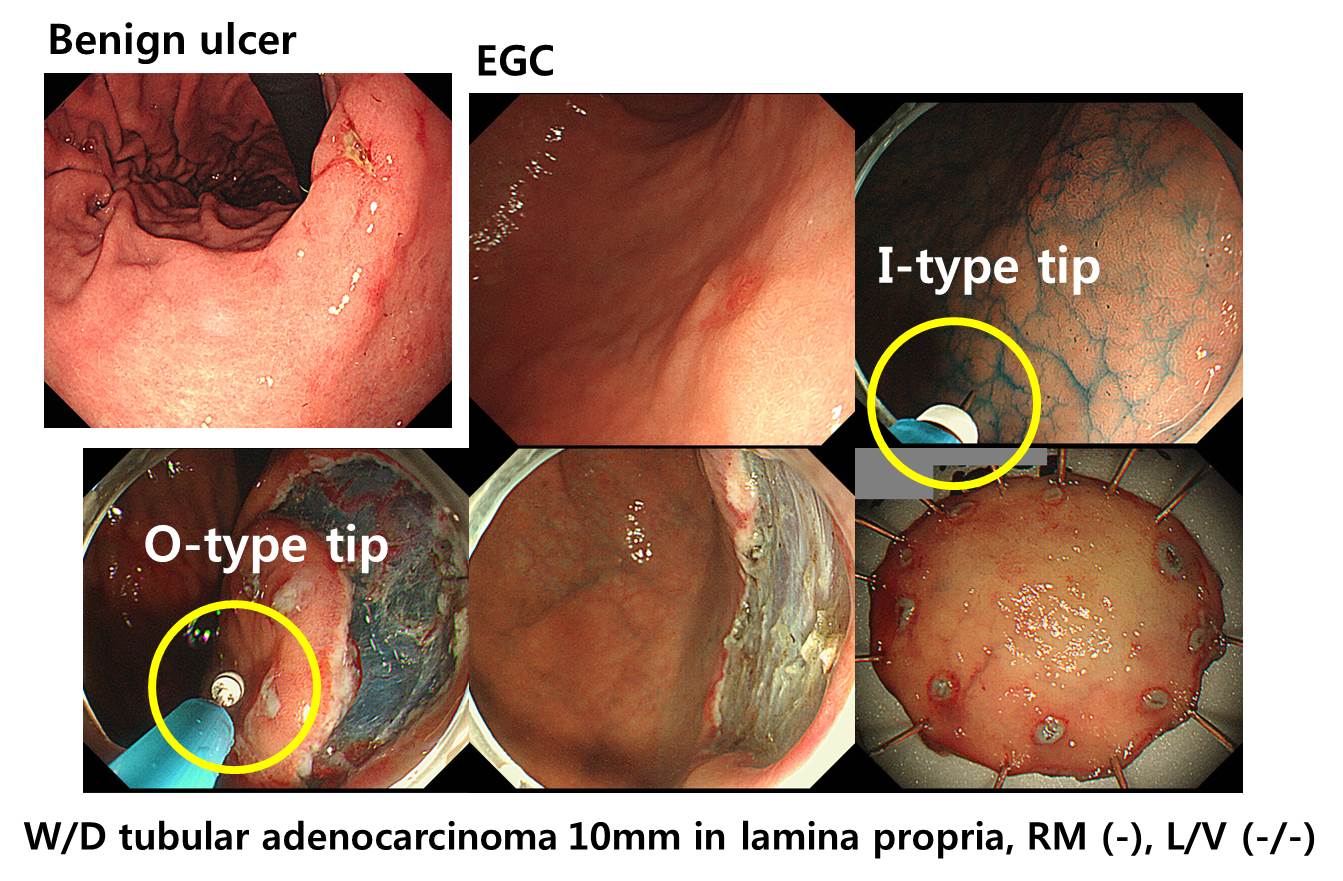 위각부 궤양과 위전정부 위암이 있었던 50대 여성입니다. 대구에 본거지를 둔 우리나라 회사인 Finemedix에서 나온 ClearCut knife H type을 사용하여 시술하였습니다. 일본 O 사의 Dual knife와 IT knife의 기능을 합친 것과 유사한 knife입니다. 먼저 (Dual knife와 비슷한) I-type tip을 내밀어 marking과 precutting을 합니다. I-type tip을 후퇴시킨 후 (IT-knife와 비슷한) O-type tip을 전진시켜 submucosal dissection을 할 수 있어서 시술 시간을 절약할 수 있었습니다. I-type tip은 Dual knife 보다 조금 가늘고 O-type tip은 classical한 IT knife보다는 조금 두껍고 IT-2 knife 보다는 조금 가늘다는 느낌을 받았습니다. 실제 측정치는 아니고 손맛이 그렇다는 말씀입니다. 나중에 회사 분들에게 물어봐야겠습니다. 실제로 그런지...
위각부 궤양과 위전정부 위암이 있었던 50대 여성입니다. 대구에 본거지를 둔 우리나라 회사인 Finemedix에서 나온 ClearCut knife H type을 사용하여 시술하였습니다. 일본 O 사의 Dual knife와 IT knife의 기능을 합친 것과 유사한 knife입니다. 먼저 (Dual knife와 비슷한) I-type tip을 내밀어 marking과 precutting을 합니다. I-type tip을 후퇴시킨 후 (IT-knife와 비슷한) O-type tip을 전진시켜 submucosal dissection을 할 수 있어서 시술 시간을 절약할 수 있었습니다. I-type tip은 Dual knife 보다 조금 가늘고 O-type tip은 classical한 IT knife보다는 조금 두껍고 IT-2 knife 보다는 조금 가늘다는 느낌을 받았습니다. 실제 측정치는 아니고 손맛이 그렇다는 말씀입니다. 나중에 회사 분들에게 물어봐야겠습니다. 실제로 그런지...
 Injector와 ESD knife를 하나의 catheter로 만든 제품(onestep ESD knife)이 우리나라에서 개발되었습니다. 매우 유용할 것으로 판단됩니다. (2019-4-11. 이준행)
Injector와 ESD knife를 하나의 catheter로 만든 제품(onestep ESD knife)이 우리나라에서 개발되었습니다. 매우 유용할 것으로 판단됩니다. (2019-4-11. 이준행)
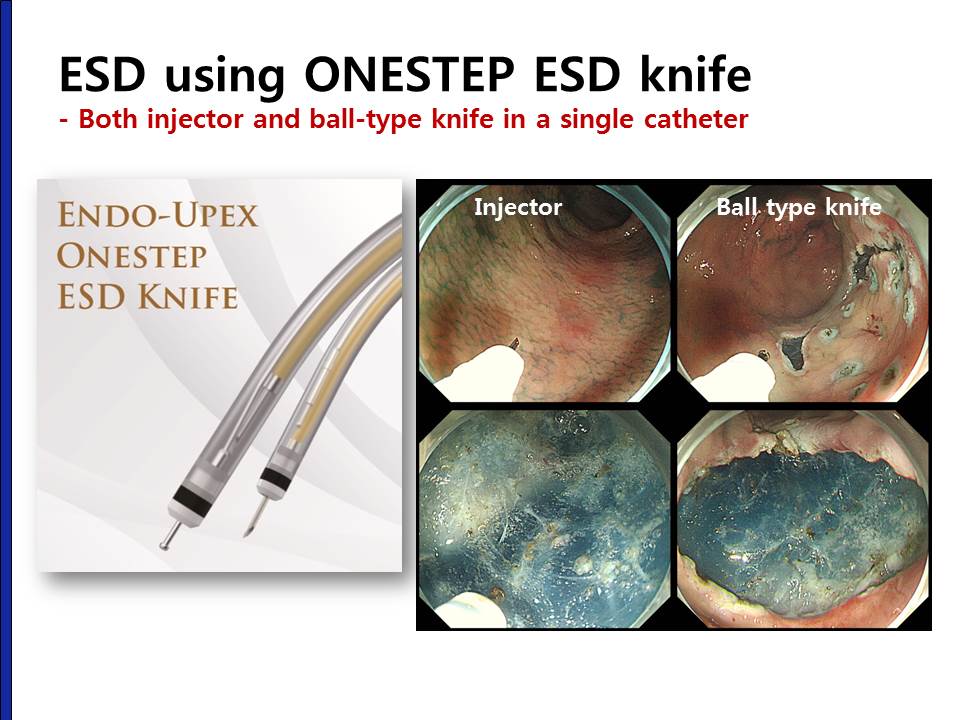 국내에서 개발된 one step ESD knife(제품설명서)를 이용한 ESD 시술입니다. Injector와 ESD knife를 하나의 catheter로 만든 제품으로 ESD 도중 knife를 넣고 빼고 하지 않고 시술할 수 있어서 매우 유용했습니다. 시간이 매우 절약되었고, assistant의 일이 많이 줄어들어 시술이 compact하게 진행된다는 느낌이었습니다. Tip이 약간 둔하다는 느낌이었은데 이는 두 개의 도구가 좁은 공간에 위치하여 어쩔 수 없는 측면이 있다는 생각이 들었습니다. 국내에서 여러 좋은 도구가 개발되고 있다는 점은 참으로 반가운 일입니다. 이 환자의 병리결과는 아래와 같았습니다.
국내에서 개발된 one step ESD knife(제품설명서)를 이용한 ESD 시술입니다. Injector와 ESD knife를 하나의 catheter로 만든 제품으로 ESD 도중 knife를 넣고 빼고 하지 않고 시술할 수 있어서 매우 유용했습니다. 시간이 매우 절약되었고, assistant의 일이 많이 줄어들어 시술이 compact하게 진행된다는 느낌이었습니다. Tip이 약간 둔하다는 느낌이었은데 이는 두 개의 도구가 좁은 공간에 위치하여 어쩔 수 없는 측면이 있다는 생각이 들었습니다. 국내에서 여러 좋은 도구가 개발되고 있다는 점은 참으로 반가운 일입니다. 이 환자의 병리결과는 아래와 같았습니다.
Stomach, ESD: Early gastric carcinoma
1. Location : antrum, posterior wall
2. Gross type : EGC type IIc
3. Histologic type : tubular adenocarcinoma, moderately differentiated
4. Histologic type by Lauren : intestinal
5. Size of carcinoma : (1) longest diameter, 8 mm (2) vertical diameter, 7 mm
6. Depth of invasion : invades mucosa (muscularis mucosa) (pT1a)
7. Resection margin : free from carcinoma(N). safety margin : distal 7 mm, proximal 6 mm, anterior 12 mm, posterior 6 mm, deep 200 ㎛
8. Lymphatic invasion : not identified(N)
9. Venous invasion : not identified(N)
10. Perineural invasion : not identified(N)
11. Pre-existing adenoma : none
12. Microscopic ulcer : absent
13. Histologic heterogeneity: absent
14. Associated finding: Gastritis cystica superficialis
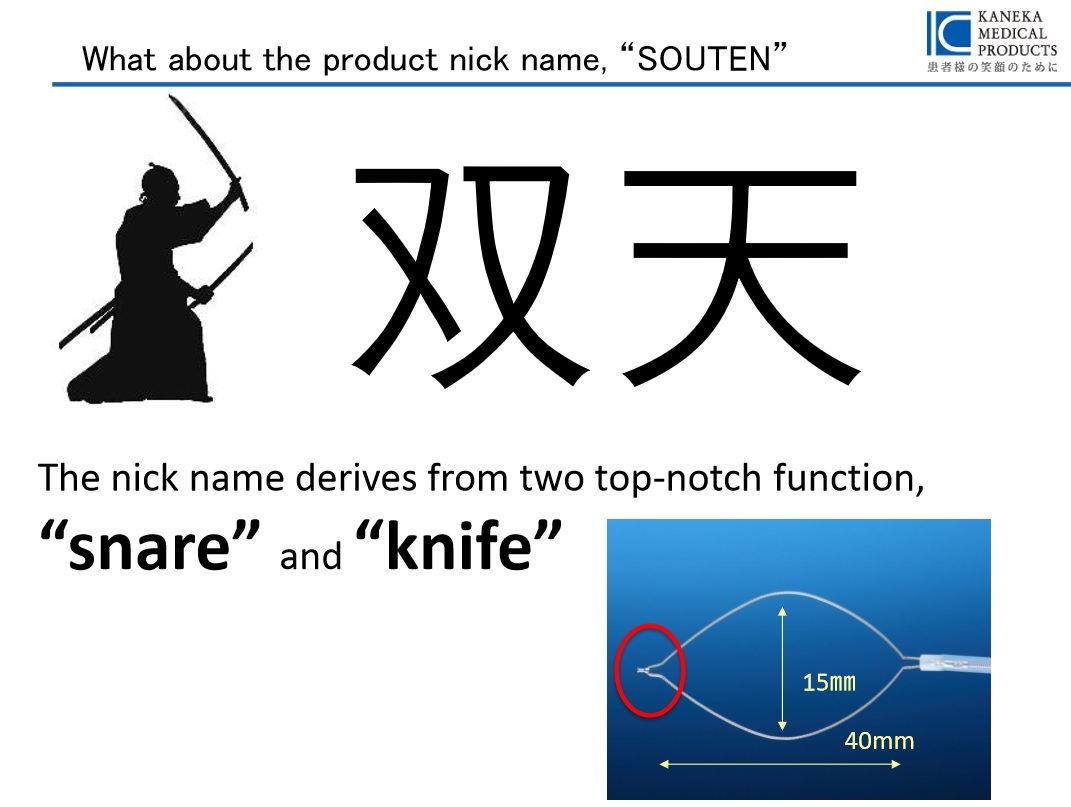 Dual knife와 snare의 특성을 조합한 새로운 knife(상품명: Souten)가 M.I.Tech를 통하여 국내에 소개되었습니다. Snare polypectomy로 치료하기에는 조금 크고, ESD를 적용하기에는 조금 작은 병소에 EMR-P를 사용할 수 있는데 Souten은 한 개의 catheter로 EMR-P를 할 수 있게 개발되었습니다. 우리나라에서는 보험등재는 ESD knife로 등재되었으므로 일반적인 EMR에서는 사용할 수 없고 ESD Knife로만 처방할 수 있다고 합니다.
Dual knife와 snare의 특성을 조합한 새로운 knife(상품명: Souten)가 M.I.Tech를 통하여 국내에 소개되었습니다. Snare polypectomy로 치료하기에는 조금 크고, ESD를 적용하기에는 조금 작은 병소에 EMR-P를 사용할 수 있는데 Souten은 한 개의 catheter로 EMR-P를 할 수 있게 개발되었습니다. 우리나라에서는 보험등재는 ESD knife로 등재되었으므로 일반적인 EMR에서는 사용할 수 없고 ESD Knife로만 처방할 수 있다고 합니다.
![]()
![]()
![]() (2019-11-7. 이준행)
(2019-11-7. 이준행)
 2019년 5월 현재 사용 가능한 knife와 그 가격표입니다. (2019-5-1)
2019년 5월 현재 사용 가능한 knife와 그 가격표입니다. (2019-5-1)
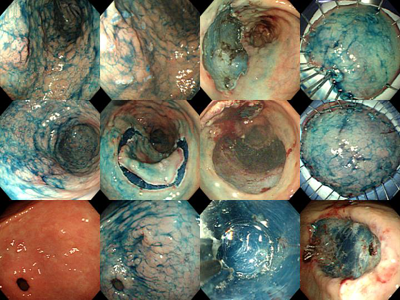 제가 초창기에 시행한 ESD 환자의 사진들입니다. ESD를 처음 시행하는 경우에는 매우 긴 시간이 소요되므로 하루에 한 환자 이상을 시술하기 어렵지만 점차 익숙해지면 한 session에 2-3명은 가능합니다. 처음에 흔히 겪게되는 합병증은 bleeding인데 저도 새벽 2시에 병원에 나와서 내시경적 지혈을 시행한 경우도 있었습니다. [2005. 1. 12.]
제가 초창기에 시행한 ESD 환자의 사진들입니다. ESD를 처음 시행하는 경우에는 매우 긴 시간이 소요되므로 하루에 한 환자 이상을 시술하기 어렵지만 점차 익숙해지면 한 session에 2-3명은 가능합니다. 처음에 흔히 겪게되는 합병증은 bleeding인데 저도 새벽 2시에 병원에 나와서 내시경적 지혈을 시행한 경우도 있었습니다. [2005. 1. 12.]
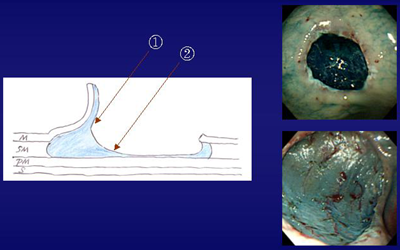 Endoscopic submucosal dissection에서 어디를 자를 것인지 결정하는 것은 쉽지 않습니다. Deep resection margin을 충분히 확보하기 위해서 가급적 점막하층을 두껍게 잘라내는 것이 좋겠으나 깊게 자를수록 시간이 오래 걸리고 천공의 위험이 증가됩니다. 그림에서 1의 위치를 dissection하는 것은 그다지 어렵지 않은 반면, 2의 위치를 dissection 하는 것은 상당히 어려운 일입니다. ESD의 초보자인 경우 합병증의 위험성 때문에 1의 위치를 선택하겠지만 전문가의 경우는 대부분 2의 위치를 선택합니다. 우측 상단의 사진은 제가 ESD를 시작할 당시의 시술 결과로 비교적 얇게 dissection이 되었다고 판단하였던 경우이며 우측 하단의 사진은 ESD의 시술예가 증가하면서 dissection을 깊게 가져간 최근의 시술 결과입니다. 절제된 표본을 손가락 끝으로 만져보아도 두께의 차이를 느낄 수 있습니다. 그러나 이러한 차이가 outcome에 영향을 주는지는 연구결과로 발표된 바가 없으므로 향후 추시가 필요한 부분입니다. [2005. 2. 12.]
Endoscopic submucosal dissection에서 어디를 자를 것인지 결정하는 것은 쉽지 않습니다. Deep resection margin을 충분히 확보하기 위해서 가급적 점막하층을 두껍게 잘라내는 것이 좋겠으나 깊게 자를수록 시간이 오래 걸리고 천공의 위험이 증가됩니다. 그림에서 1의 위치를 dissection하는 것은 그다지 어렵지 않은 반면, 2의 위치를 dissection 하는 것은 상당히 어려운 일입니다. ESD의 초보자인 경우 합병증의 위험성 때문에 1의 위치를 선택하겠지만 전문가의 경우는 대부분 2의 위치를 선택합니다. 우측 상단의 사진은 제가 ESD를 시작할 당시의 시술 결과로 비교적 얇게 dissection이 되었다고 판단하였던 경우이며 우측 하단의 사진은 ESD의 시술예가 증가하면서 dissection을 깊게 가져간 최근의 시술 결과입니다. 절제된 표본을 손가락 끝으로 만져보아도 두께의 차이를 느낄 수 있습니다. 그러나 이러한 차이가 outcome에 영향을 주는지는 연구결과로 발표된 바가 없으므로 향후 추시가 필요한 부분입니다. [2005. 2. 12.]
ESD는 single hand surgery입니다. Working channel을 통하여 ESD knife를 내밀어 병소를 절제하기 때문입니다. 일본에서는 두 개의 내시경을 삽입하여 시술하는 의사도 있다는 이야기를 듣기도 했지만 한 환자에게 두 개의 내시경을 삽입하는 것은 간단한 일이 아닙니다. Two hand surgery를 흉내내기 위하여 여러 시도가 있었지만 최근에는 traction method가 유용하게 사용되고 있습니다.
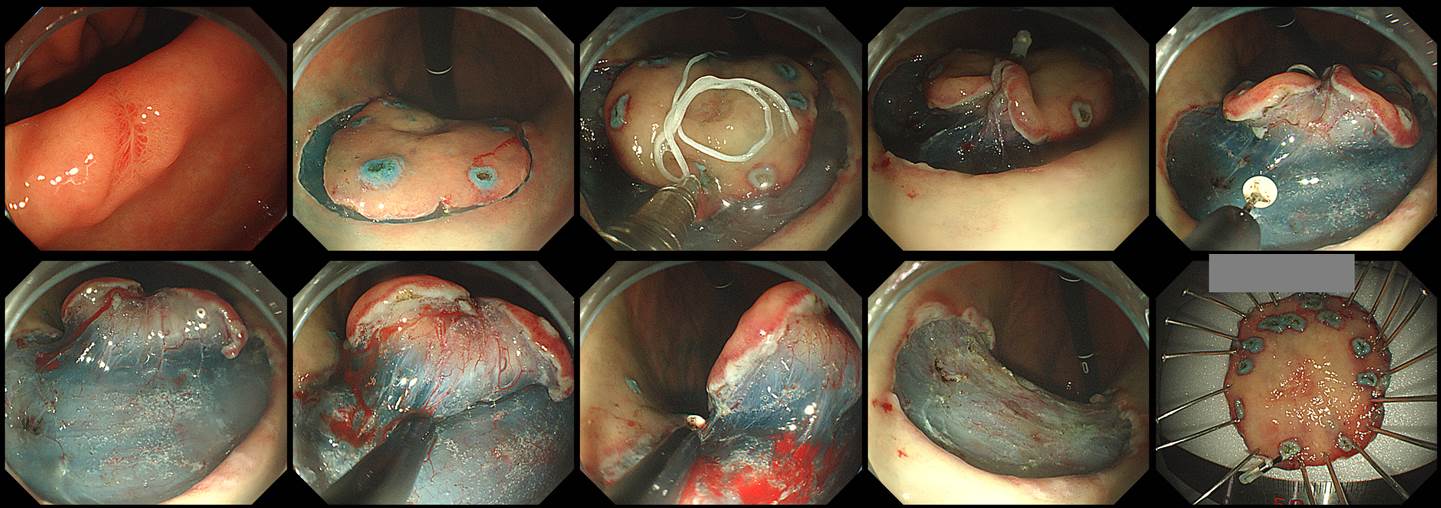 위각이나 위체하부 소만 병소는 ESD가 쉽지 않습니다. Submucosal dissection 과정에서 submucosal layer가 잘 노출되지 않는 경우가 많기 때문입니다. 이럴 때는 traction ESD가 딱입니다. Circumferential cutting 후 실을 연결한 clip을 병소의 proximal에 장착하고 실을 살살 당기면 submucosal layer가 아주 잘 보이게 되므로 시술이 쉬워집니다. 맨 마지막 사진을 보시면 수거한 specimen의 distal end에 clip이 장착되어 있고 실이 연결된 모습니다. 병리 결과는 아래와 같았습니다. [2019-7-14]
위각이나 위체하부 소만 병소는 ESD가 쉽지 않습니다. Submucosal dissection 과정에서 submucosal layer가 잘 노출되지 않는 경우가 많기 때문입니다. 이럴 때는 traction ESD가 딱입니다. Circumferential cutting 후 실을 연결한 clip을 병소의 proximal에 장착하고 실을 살살 당기면 submucosal layer가 아주 잘 보이게 되므로 시술이 쉬워집니다. 맨 마지막 사진을 보시면 수거한 specimen의 distal end에 clip이 장착되어 있고 실이 연결된 모습니다. 병리 결과는 아래와 같았습니다. [2019-7-14]
ESD: Early gastric carcinoma
1. Location : angle, lesser curvature
2. Gross type : EGC type IIc
3. Histologic type : tubular adenocarcinoma, moderately differentiated (70%) >> signet ring cell carcinoma (30%)
4. Histologic type by Lauren : intestinal
5. Size of carcinoma : (1) longest diameter, 10 mm (2) vertical diameter, 3 mm
6. Depth of invasion : invades mucosa (lamina propria) (pT1a)
7. Resection margin : free from carcinoma(N), safety margin : distal 8 mm, proximal 17 mm, anterior 8 mm, posterior 12 mm, deep 500 ㎛
8. Lymphatic invasion : not identified(N)
9. Venous invasion : not identified(N)
10. Perineural invasion : not identified(N)
11. Microscopic ulcer : absent
12. Histologic heterogeneity: present
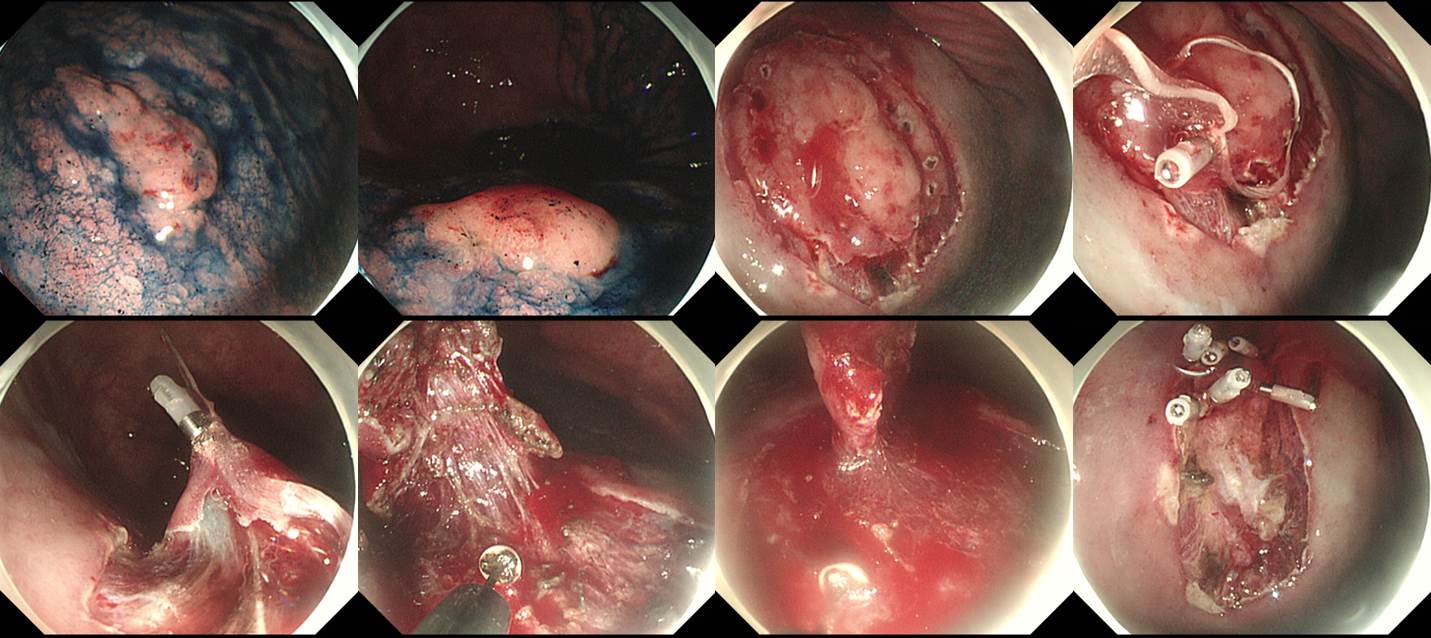 위 증례와 거의 비슷한 경우입니다. Traction ESD를 시행하여 비교적 빠르고 안전하게 시술할 수 있었습니다.
위 증례와 거의 비슷한 경우입니다. Traction ESD를 시행하여 비교적 빠르고 안전하게 시술할 수 있었습니다.
ESD: Early gastric carcinoma
1. Location : high body, greater curvature
2. Gross type : EGC type IIa
3. Histologic type : tubular adenocarcinoma, moderately differentiated
4. Histologic type by Lauren : intestinal
5. Size of carcinoma : (1) longest diameter, 22 mm (2) vertical diameter, 14 mm
6. Depth of invasion : invades mucosa (muscularis mucosa) (pT1a)
7. Resection margin : free from carcinoma(N)
8. Lymphatic invasion : not identified(N)
9. Venous invasion : not identified(N)
10. Perineural invasion : not identified(N)
11. Pre-existing adenoma : none
12. Microscopic ulcer : absent
13. Histologic heterogeneity: absent
14. Associated finding: Gastritis cystica superficialis
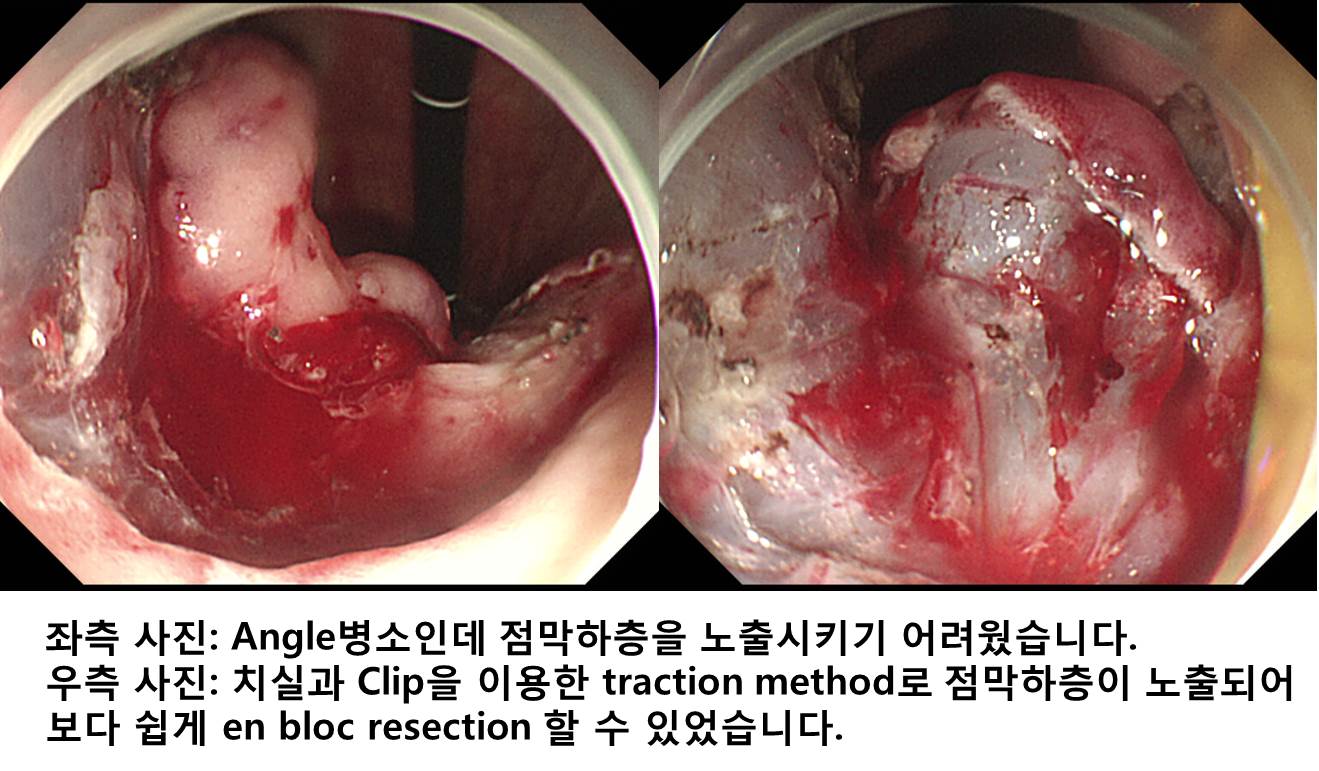 위각부 선종 내시경 치료 후 재발로 시행한 ESD였습니다. Dual knife로 circumferential cutting을 하였고 IT-2 knife로 submucosal dissection을 시도하였으나 병소의 위치와 submucosal fibrosis로 인하여 cutting을 위한 점막하층 노출이 어려웠습니다. 치실과 clip으로 traction을 하였고 점막하층이 충분히 노출되어 훨씬 용이하게 submucosal dissection을 할 수 있었습니다. 최종 병리결과는 well differentiated tubular adenocarcinoma, 22mm, MM invasion, lateral margin (-), L/V (-/-) 로 나왔습니다. 다소 고생스러웠지만 one piece resection을 위하여 노력한 보람이 있다는 생각이 들었습니다.
위각부 선종 내시경 치료 후 재발로 시행한 ESD였습니다. Dual knife로 circumferential cutting을 하였고 IT-2 knife로 submucosal dissection을 시도하였으나 병소의 위치와 submucosal fibrosis로 인하여 cutting을 위한 점막하층 노출이 어려웠습니다. 치실과 clip으로 traction을 하였고 점막하층이 충분히 노출되어 훨씬 용이하게 submucosal dissection을 할 수 있었습니다. 최종 병리결과는 well differentiated tubular adenocarcinoma, 22mm, MM invasion, lateral margin (-), L/V (-/-) 로 나왔습니다. 다소 고생스러웠지만 one piece resection을 위하여 노력한 보람이 있다는 생각이 들었습니다.
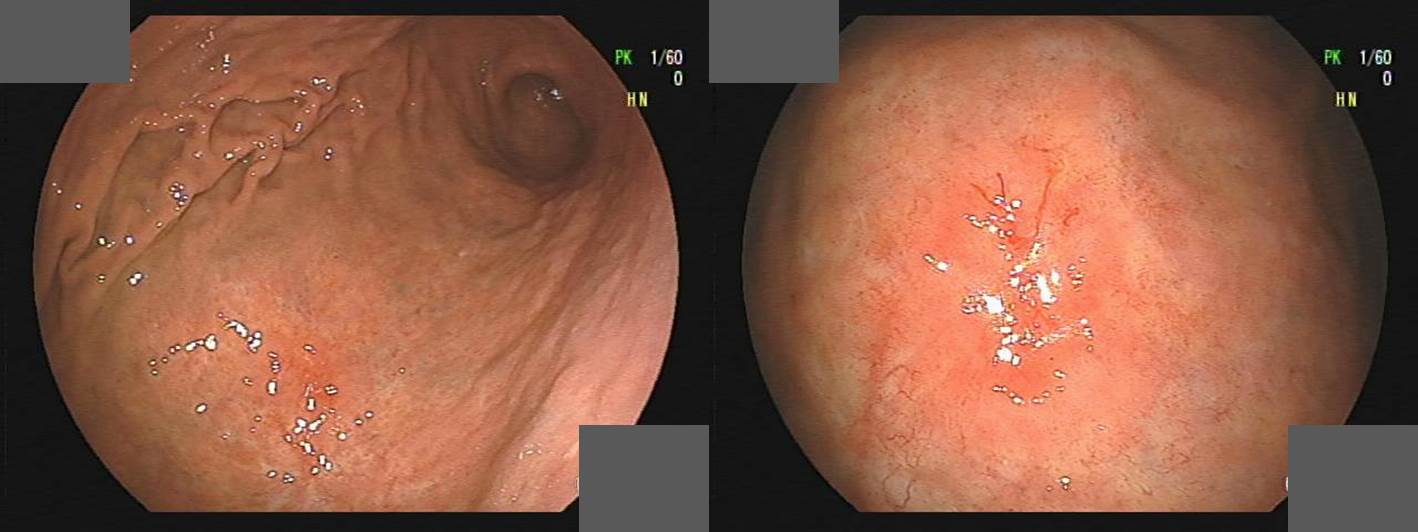

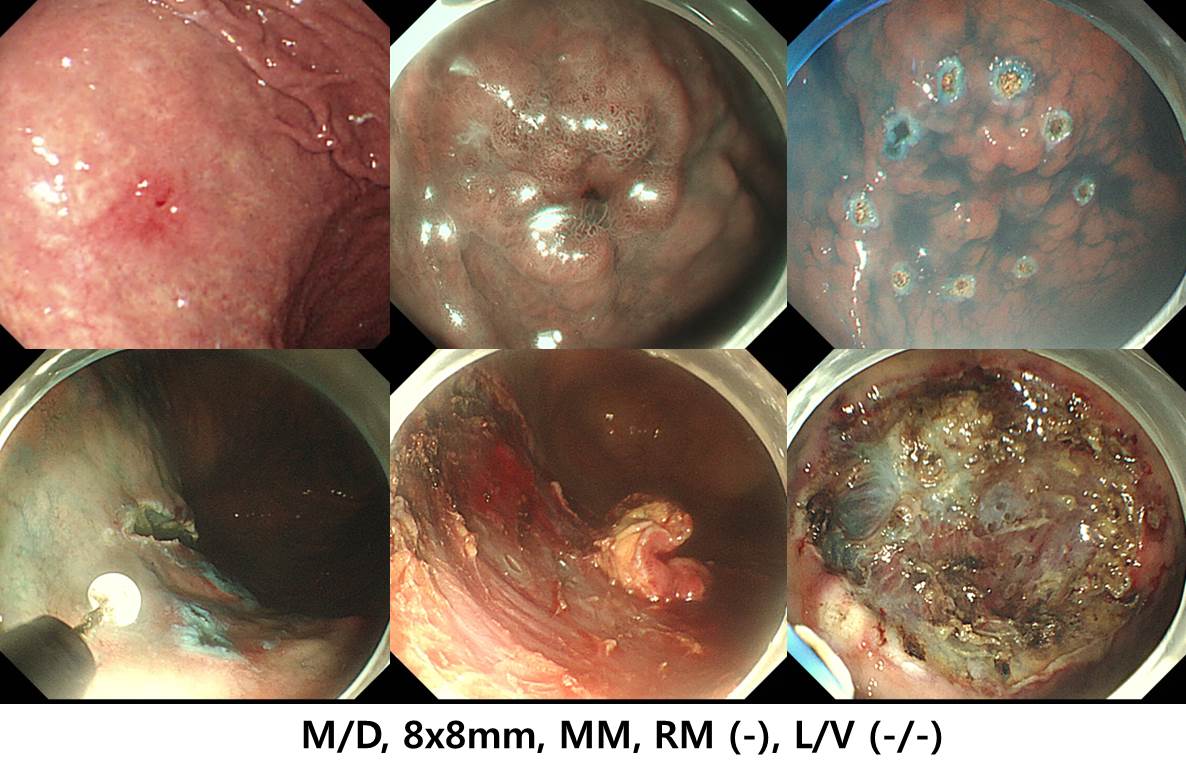 ESD를 위해서는 병소와 평행한 방향으로 접근해야 하는데 (저는 '낮은 포복'이라고 부릅니다), 위체상부 대만서는 낮은 포복 접근이 매우 까다롭습니다. 크게 반전하면서 잘 비틀어 각도를 맞춰야 합니다. 이런 시술을 하고 나면 손가락, 손목, 어깨, 허리가 모두 저리고 아픕니다. 걱정스러운 마음으로 stretching을 하면서 결과를 기다립니다. 앞으로 이런 병소는 수술을 보내야겠다 생각합니다. 며칠 후 추가 수술을 권하지 않아도 좋을 병리결과가 나오면 그 동안의 통증이 씻은 듯이 사라집니다. "앞으로 이런 병소는 수술을 보내야지" 다짐했던 것은 없던 일이 됩니다. 고생스럽더라도 또 하는 수 밖에... [2018-8-19] → Traction ESD를 시도하면 잘 해결될 수 있는 증례일 것 같습니다. [2019-7-14]
ESD를 위해서는 병소와 평행한 방향으로 접근해야 하는데 (저는 '낮은 포복'이라고 부릅니다), 위체상부 대만서는 낮은 포복 접근이 매우 까다롭습니다. 크게 반전하면서 잘 비틀어 각도를 맞춰야 합니다. 이런 시술을 하고 나면 손가락, 손목, 어깨, 허리가 모두 저리고 아픕니다. 걱정스러운 마음으로 stretching을 하면서 결과를 기다립니다. 앞으로 이런 병소는 수술을 보내야겠다 생각합니다. 며칠 후 추가 수술을 권하지 않아도 좋을 병리결과가 나오면 그 동안의 통증이 씻은 듯이 사라집니다. "앞으로 이런 병소는 수술을 보내야지" 다짐했던 것은 없던 일이 됩니다. 고생스럽더라도 또 하는 수 밖에... [2018-8-19] → Traction ESD를 시도하면 잘 해결될 수 있는 증례일 것 같습니다. [2019-7-14]
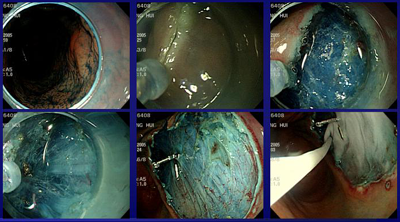 Flex knife를 이용한 ESD의 예입니다. ESD 초기에 동경대학교 Yahagi 교수님께서 개발하여 Olympus에서 시판된 ESD 절개도였습니다. 너무 낭창낭창하여 조금 길게 내밀면 조절이 어렵다는 단점이 지적되었고, 이후 마찬가지로 Yahagi 교수님이 개발한 Dual knife로 대체되었습니다.
Flex knife를 이용한 ESD의 예입니다. ESD 초기에 동경대학교 Yahagi 교수님께서 개발하여 Olympus에서 시판된 ESD 절개도였습니다. 너무 낭창낭창하여 조금 길게 내밀면 조절이 어렵다는 단점이 지적되었고, 이후 마찬가지로 Yahagi 교수님이 개발한 Dual knife로 대체되었습니다.
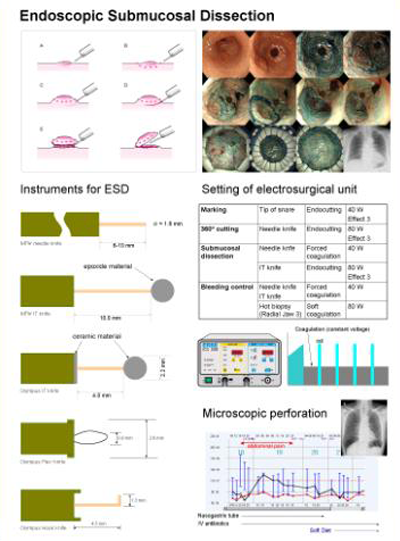 ESD는 우리나라에서 아직 보편적으로 시행되지 않고 있는 신기술이며, 이에 대하여 익숙한 의료진이 많지 않습니다. 저는 개인적으로 내시경실에 그림과 같은 도표를 만들어서 붙여두고 사용하고 있습니다. setting 등에 대한 자세히 기록을 해놓았기 때문에 보조자에게 도움이 되는 것은 당연하고 학생과 전공의들의 교육자료로도 유용합니다. [2004. 11. 17]
ESD는 우리나라에서 아직 보편적으로 시행되지 않고 있는 신기술이며, 이에 대하여 익숙한 의료진이 많지 않습니다. 저는 개인적으로 내시경실에 그림과 같은 도표를 만들어서 붙여두고 사용하고 있습니다. setting 등에 대한 자세히 기록을 해놓았기 때문에 보조자에게 도움이 되는 것은 당연하고 학생과 전공의들의 교육자료로도 유용합니다. [2004. 11. 17]
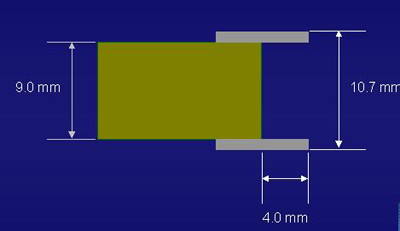 EMR, 특히 ESD를 할 때 병소가 내시경 tip에 너무 근접하면 시야확보가 어렵습니다. 따라서 내시경 tip에 soft type의 transparent hood를 장착하면 크게 도움이 됩니다. 적당한 거리를 유지할 수 있으므로 다양한 각도로 병소에 접근할 수 있습니다. 근접촬영에도 도움이 됩니다. Needle knife를 이용한 (일본에서는 Flex knife를 이용하고 있음) direct한 방식의 submucosal dissection을 시행할 때 점막하조직을 최대한 노출시킬 수 있으므로 거의 필수적인 장비입니다. 과거부터 필요성이 제기되고 있었으나 최근까지 국내에 수입되지 않아 EMR 시술에 어려움이 적지 않았습니다. 마침내 2004년 11월 품목허가가 떨어져서 수입이 시작되었습니다. 돌출부의 길이가 2 mm 인 모델과 4 mm 인 모델이 있는데 통상 4 mm 길이가 보다 널리 사용되고 있습니다. 내시경 외경에 따라 모델명이 다르므로 주문할 경우에 자신이 사용하는 내시경에 맞는지 확인할 필요가 있습니다. 제가 주로 사용하는 내시경은 GIF-Q260과 GIF-XQ240인데 두 모델 모두 D-201-10704를 사용하므로 저희 병원에서는 이 한가지 hood 만을 이용하고 있습니다.[2004. 11. 23.]
EMR, 특히 ESD를 할 때 병소가 내시경 tip에 너무 근접하면 시야확보가 어렵습니다. 따라서 내시경 tip에 soft type의 transparent hood를 장착하면 크게 도움이 됩니다. 적당한 거리를 유지할 수 있으므로 다양한 각도로 병소에 접근할 수 있습니다. 근접촬영에도 도움이 됩니다. Needle knife를 이용한 (일본에서는 Flex knife를 이용하고 있음) direct한 방식의 submucosal dissection을 시행할 때 점막하조직을 최대한 노출시킬 수 있으므로 거의 필수적인 장비입니다. 과거부터 필요성이 제기되고 있었으나 최근까지 국내에 수입되지 않아 EMR 시술에 어려움이 적지 않았습니다. 마침내 2004년 11월 품목허가가 떨어져서 수입이 시작되었습니다. 돌출부의 길이가 2 mm 인 모델과 4 mm 인 모델이 있는데 통상 4 mm 길이가 보다 널리 사용되고 있습니다. 내시경 외경에 따라 모델명이 다르므로 주문할 경우에 자신이 사용하는 내시경에 맞는지 확인할 필요가 있습니다. 제가 주로 사용하는 내시경은 GIF-Q260과 GIF-XQ240인데 두 모델 모두 D-201-10704를 사용하므로 저희 병원에서는 이 한가지 hood 만을 이용하고 있습니다.[2004. 11. 23.]
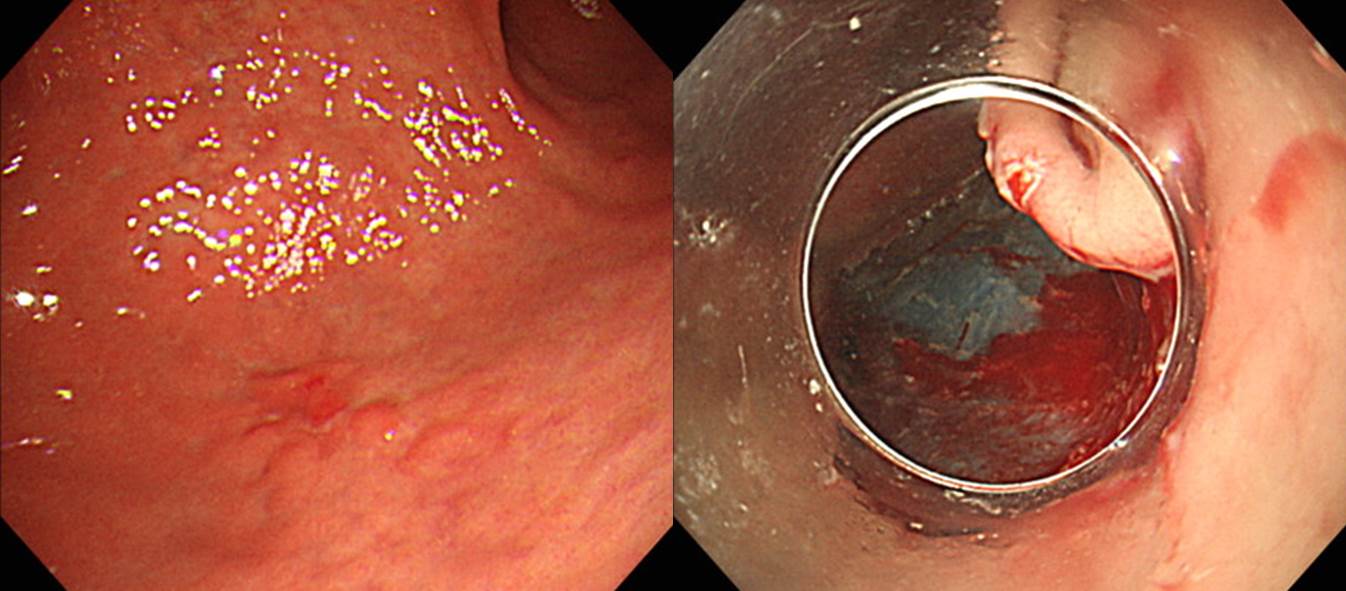 Hood를 너무 길게 내민 경우입니다. 시야가 충분히 확보되지 않기 때문에 불편할 수 있습니다. 조금 짧은 hood 사용을 권합니다. [2018. 4. 5.]
Hood를 너무 길게 내민 경우입니다. 시야가 충분히 확보되지 않기 때문에 불편할 수 있습니다. 조금 짧은 hood 사용을 권합니다. [2018. 4. 5.]
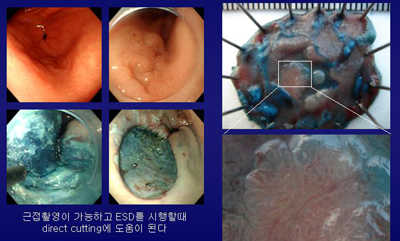
위 그림은 돌출부 길이 4mm인 transparent hood를 이용한 실제 장면입니다. 병소의 근접촬영과 direct submucosal dissection에서의 유용성을 쉽게 알 수 있습니다.
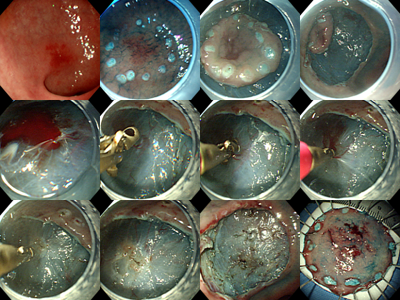 EMR에서는 hot biopsy forcep을 이용한 지혈이 자주 이용됩니다. 원래 hot biopsy forcep은 colon의 5 mm 정도의 작은 용종을 submucosal injection 없이 절제하는 용도로 많이 이용됩니다. 용종을 잡기 위하여 hot biopsy forcep은 통상 cup size는 어느 정도 이상의 크기가 됩니다. 그러나 cup size가 작은 hot biopsy forcep은 EMR에서 active bleeding이 있어 hemostasis를 하는 경우나 절제 도중 큰 혈관이 보여 preemptive hemostasis를 하는 경우 매우 유용합니다. 이때에는 vessel과 주변조직을 잡고 hot biopsy forcep을 약간 당긴상태에서 coagulation current를 조금씩 여러번에 나누어 통과시키는 방법을 사용합니다. 너무 많은 조직을 잡고 많은 양의 전류를 통과시키면 muscle layer와 serosal layer에 burn이 발생하여 때로는 치명적일 수 있는 delayed perforation이 발생할 수 있으므로 주의를 해야 합니다. 개인적으로는 hot biopsy forcep은 Boston 사의 Radial Jaw 3라는 모델을 사용하고 있으며, ERBE ICC200에서 Soft coagulation current 100 Watt를 기본 setting으로 하고 있습니다. 강조하건데 (1) cup size가 큰 hot biopsy forcep을 hemostasis 용도로 사용하면 위험하고, (2) coagulation을 지나치게 많이 하면 delayed perforation이 발생할 수 있습니다. [2005. 1. 7.]
EMR에서는 hot biopsy forcep을 이용한 지혈이 자주 이용됩니다. 원래 hot biopsy forcep은 colon의 5 mm 정도의 작은 용종을 submucosal injection 없이 절제하는 용도로 많이 이용됩니다. 용종을 잡기 위하여 hot biopsy forcep은 통상 cup size는 어느 정도 이상의 크기가 됩니다. 그러나 cup size가 작은 hot biopsy forcep은 EMR에서 active bleeding이 있어 hemostasis를 하는 경우나 절제 도중 큰 혈관이 보여 preemptive hemostasis를 하는 경우 매우 유용합니다. 이때에는 vessel과 주변조직을 잡고 hot biopsy forcep을 약간 당긴상태에서 coagulation current를 조금씩 여러번에 나누어 통과시키는 방법을 사용합니다. 너무 많은 조직을 잡고 많은 양의 전류를 통과시키면 muscle layer와 serosal layer에 burn이 발생하여 때로는 치명적일 수 있는 delayed perforation이 발생할 수 있으므로 주의를 해야 합니다. 개인적으로는 hot biopsy forcep은 Boston 사의 Radial Jaw 3라는 모델을 사용하고 있으며, ERBE ICC200에서 Soft coagulation current 100 Watt를 기본 setting으로 하고 있습니다. 강조하건데 (1) cup size가 큰 hot biopsy forcep을 hemostasis 용도로 사용하면 위험하고, (2) coagulation을 지나치게 많이 하면 delayed perforation이 발생할 수 있습니다. [2005. 1. 7.]
 좌측이 colon에서 주로 사용하는 hot biopsy forcep이고 우측이 제가 bleeding control을 위하여 사용하는 hot biopsy forcep입니다. Bleeding control을 위해서는 cup opening을 섬세하게 control할 수 있는 것이 좋으며 cup이 지나차게 크지 않은 것이 좋습니다. [2005. 2. 11.]
좌측이 colon에서 주로 사용하는 hot biopsy forcep이고 우측이 제가 bleeding control을 위하여 사용하는 hot biopsy forcep입니다. Bleeding control을 위해서는 cup opening을 섬세하게 control할 수 있는 것이 좋으며 cup이 지나차게 크지 않은 것이 좋습니다. [2005. 2. 11.]
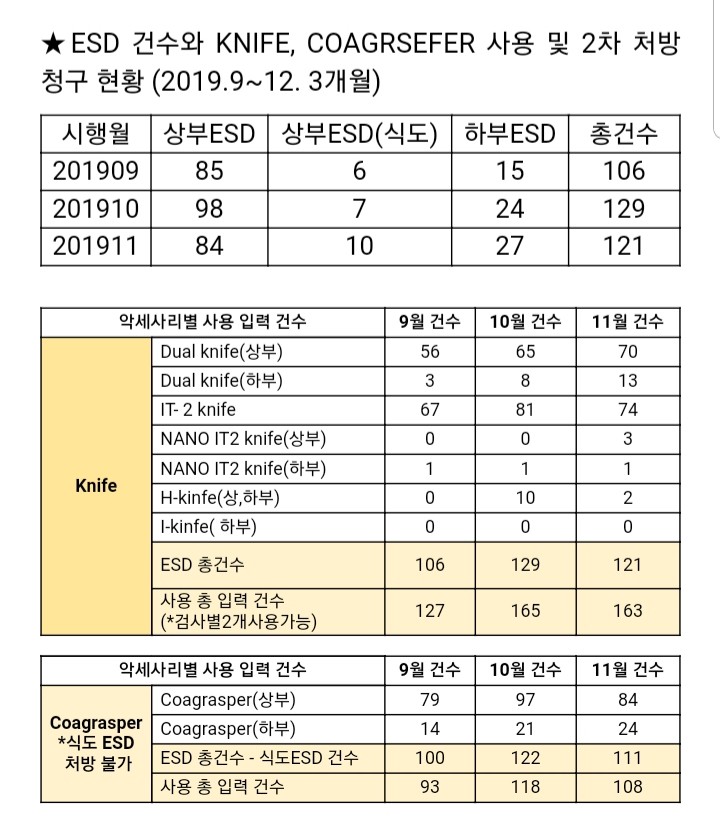 ESD를 후 대부분 Coagrasper를 사용합니다. 저희 병원의 실제 자료입니다. ESD 건수 대비 90% 이상입니다. [2019-12-8]
ESD를 후 대부분 Coagrasper를 사용합니다. 저희 병원의 실제 자료입니다. ESD 건수 대비 90% 이상입니다. [2019-12-8]
 Coagrasper가 조금씩 성능을 개선하고 있습니다. [2021-5-4]
Coagrasper가 조금씩 성능을 개선하고 있습니다. [2021-5-4]
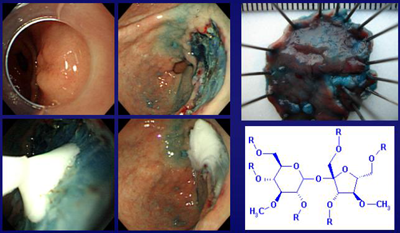 EMR로 인한 artifical ulcer에서의 bleeding을 막기 위한 가장 좋은 방법은 EMR 시술 도중 눈에 보이는 모든 active bleeding을 hot biopsy forcep등의 여러가지 도구를 이용하여 확실히 조절하는 것입니다. 물론 electrocauterization이 너무 지나치면 transmural burn에 의하여 fatal complication의 하나인 delayed perforation이 발생할 수 있으므로 주의를 해야 합니다. 또한 active bleeding이 없는 병소라고 하더라고 vessel이 현저히 노출되어 보이는 경우에는 electrocauterization을 해 주는 것이 좋습니다. 저는 이러한 과정을 "preemptive hemostasis"라고 부르고 있으며 과거에는 heat probe를 이용하여 눌러주는 방법을 사용하다가 ("ironing method"라고 명명하였습니다) 최근에는 hot biopsy forcep을 이용하고 있습니다. 이러한 preemtive hemostasis가 과연 효과적인지에 대한 연구를 시행하기는 거의 불가능하므로 정확한 data를 제시할 수는 없습니다. 그렇지만 저의 짧은 경험으로는 매우 도움이 된다고 생각합니다. Bleeding control이 다 끝난 ulcer base에 여러가지 약제를 뿌림으로써 재출혈을 막으려는 다양한 시도가 있습니다. 국내에서는 thrombin이나 ALTO spray가 흔하게 사용되고 있으며 일본에서는 Cleantop이라는 내시경소독기로 유명한 Kaigen사에서 나오는 ACIDLESS solution이 널리 이용되고 있습니다. ACIDLESS의 성분은 100 ml 중 "수산화알루미늄 gel 56 g (수산화알루미늄으로 2.24 g) + 수산화마그네슘 베이스 12.9 g (수산화 마그네슘으로 4.0 g)" 입니다. Sucralfate도 이러한 용도로 사용될 수 있습니다. 2004년 EMR ulcer 에 대한 sucralfate의 selective adherence에 대한 연구가 J Int Med Res라는 잡지에 실리기도 하였습니다. 저는 30 ml 주사기에 sucralfate를 1-2 pack 부어넣은 후 도포를 하고 있습니다. 이때 sucralfate의 높은 viscosity때문에 일반 spraying catheter로는 도포가 되지 않습니다. 따라서 색소살포를 위한 spraying catheter의 nozzle을 가위로 잘라내고 spraying catheter 내부의 가는 철사를 빼서 sucralfate 도포에 이용하고 있습니다. [2005. 2. 5.]
EMR로 인한 artifical ulcer에서의 bleeding을 막기 위한 가장 좋은 방법은 EMR 시술 도중 눈에 보이는 모든 active bleeding을 hot biopsy forcep등의 여러가지 도구를 이용하여 확실히 조절하는 것입니다. 물론 electrocauterization이 너무 지나치면 transmural burn에 의하여 fatal complication의 하나인 delayed perforation이 발생할 수 있으므로 주의를 해야 합니다. 또한 active bleeding이 없는 병소라고 하더라고 vessel이 현저히 노출되어 보이는 경우에는 electrocauterization을 해 주는 것이 좋습니다. 저는 이러한 과정을 "preemptive hemostasis"라고 부르고 있으며 과거에는 heat probe를 이용하여 눌러주는 방법을 사용하다가 ("ironing method"라고 명명하였습니다) 최근에는 hot biopsy forcep을 이용하고 있습니다. 이러한 preemtive hemostasis가 과연 효과적인지에 대한 연구를 시행하기는 거의 불가능하므로 정확한 data를 제시할 수는 없습니다. 그렇지만 저의 짧은 경험으로는 매우 도움이 된다고 생각합니다. Bleeding control이 다 끝난 ulcer base에 여러가지 약제를 뿌림으로써 재출혈을 막으려는 다양한 시도가 있습니다. 국내에서는 thrombin이나 ALTO spray가 흔하게 사용되고 있으며 일본에서는 Cleantop이라는 내시경소독기로 유명한 Kaigen사에서 나오는 ACIDLESS solution이 널리 이용되고 있습니다. ACIDLESS의 성분은 100 ml 중 "수산화알루미늄 gel 56 g (수산화알루미늄으로 2.24 g) + 수산화마그네슘 베이스 12.9 g (수산화 마그네슘으로 4.0 g)" 입니다. Sucralfate도 이러한 용도로 사용될 수 있습니다. 2004년 EMR ulcer 에 대한 sucralfate의 selective adherence에 대한 연구가 J Int Med Res라는 잡지에 실리기도 하였습니다. 저는 30 ml 주사기에 sucralfate를 1-2 pack 부어넣은 후 도포를 하고 있습니다. 이때 sucralfate의 높은 viscosity때문에 일반 spraying catheter로는 도포가 되지 않습니다. 따라서 색소살포를 위한 spraying catheter의 nozzle을 가위로 잘라내고 spraying catheter 내부의 가는 철사를 빼서 sucralfate 도포에 이용하고 있습니다. [2005. 2. 5.]
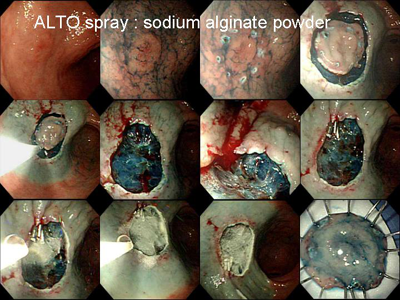 ALTO spray도 간혹 사용할 수 있습니다. 물에 닿으면 즉시 굳어지는 특성을 이용하는 것인데 이때문에 시술 도중 catheter가 막혀서 분무가 잘 안되는 경우가 있습니다. 따라서 분무 전에 내시경의 working channel을 확실하게 말리는 것이 좋습니다. 이를 위하여 저는 ALTO spray 용 catheter를 넣기 전에 50 ml 주사기로 건조한 공기를 여러번 통과시키는 방법을 이용하고 있습니다. [2005. 2. 5.]
ALTO spray도 간혹 사용할 수 있습니다. 물에 닿으면 즉시 굳어지는 특성을 이용하는 것인데 이때문에 시술 도중 catheter가 막혀서 분무가 잘 안되는 경우가 있습니다. 따라서 분무 전에 내시경의 working channel을 확실하게 말리는 것이 좋습니다. 이를 위하여 저는 ALTO spray 용 catheter를 넣기 전에 50 ml 주사기로 건조한 공기를 여러번 통과시키는 방법을 이용하고 있습니다. [2005. 2. 5.]
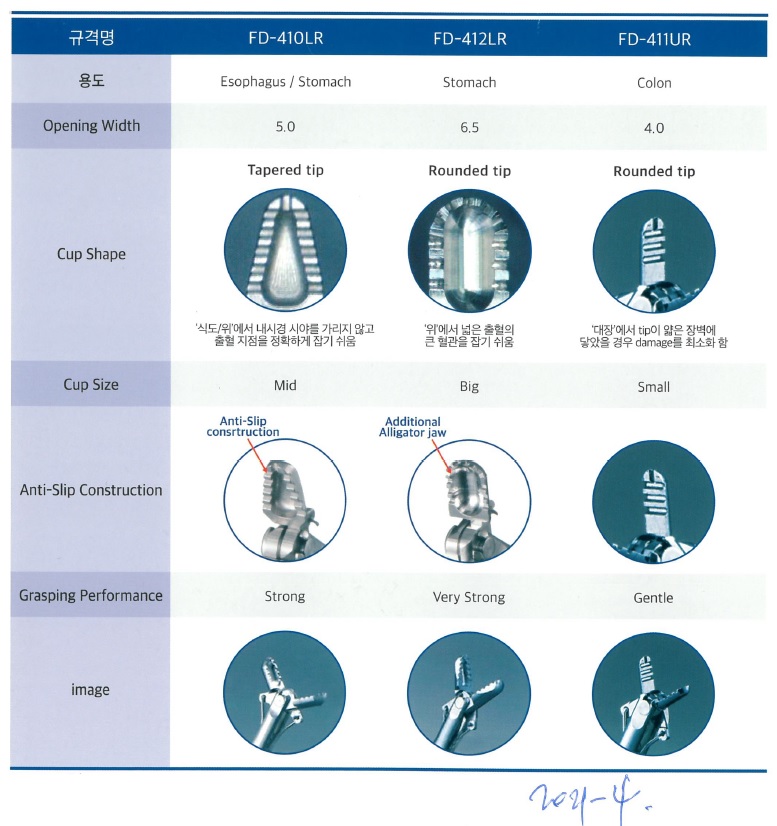
 과거 strip biopsy나 EMR-C를 주로 시행할 때에는 절제된 병소의 크기가 작아서 biopsy forcep이나 tripod (FG-45L-1)혹은 net를 이용하여 절제된 조직을 회수할 수 있습니다. 그러나 ESD를 이용하여 수 cm 이상 되는 큰 병소를 회수할 때에는 rat tooth with alligator jaws (FG-42L-1, FG-47L-1)를 이용하는 것이 좋습니다. 이러한 종류의 grasping forcep을 이용하여 암 병소가 손상되지 않도록 절제된 표면의 한쪽 가장자리를 잡고 내시경과 함께 절제된 표본을 꺼내는 것이 편리합니다. 간혹 아주 크지 않은 병소는 grasping forcep을 이용하지 않고도 suction을 이용하여 내시경의 hood 안으로 절제표본을 끌어 당긴 후 회수할 수 있으나 이 때에는 표본에 손상이 옵니다. [2005-4-1]
과거 strip biopsy나 EMR-C를 주로 시행할 때에는 절제된 병소의 크기가 작아서 biopsy forcep이나 tripod (FG-45L-1)혹은 net를 이용하여 절제된 조직을 회수할 수 있습니다. 그러나 ESD를 이용하여 수 cm 이상 되는 큰 병소를 회수할 때에는 rat tooth with alligator jaws (FG-42L-1, FG-47L-1)를 이용하는 것이 좋습니다. 이러한 종류의 grasping forcep을 이용하여 암 병소가 손상되지 않도록 절제된 표면의 한쪽 가장자리를 잡고 내시경과 함께 절제된 표본을 꺼내는 것이 편리합니다. 간혹 아주 크지 않은 병소는 grasping forcep을 이용하지 않고도 suction을 이용하여 내시경의 hood 안으로 절제표본을 끌어 당긴 후 회수할 수 있으나 이 때에는 표본에 손상이 옵니다. [2005-4-1]
한 동안 net를 이용하여 절제표본을 회수하는 방법이 많이 씌였습니다. 그러나 (아마도 2017년부터) net의 사용이 이물제거술로 한정되는 바람에 ESD specimen에서 net를 사용하지 못하게 되었습니다. 그래서 suction으로 절제표본을 내시경 tip으로 당겨서 제거하고 있습니다. 그러나 매우 위험한 방법입니다. 드물게 ESD 절제 표본이 airway로 넘어가 arrest가 발생할 수 있기 때문입니다. 하인리히 방법을 적용하여 가까스로 환자의 목숨을 건진 경우도 보았습니다. 의사들이 환자를 위하여 적절하게 net를 사용할 수 있도록 허용해야 할 것입니다. [2019-7-20]

 그림과 같이 시술 도중에 육안적으로 관찰되는 frank perforation이 있는 경우에는 내시경적 치료의 적응증이 됩니다. 대부분의 경우 clip을 이용하여 perforation을 직접 closure하면 수술적 치료 없이 호전되는 경우가 많습니다. 이처럼 내시경적 치료를 시행한 frank perforation에서 언제 diet를 시작하여야 하는가에 대한 정해진 원칙은 없으나 앞서 언급한 microperforation과 동일한 방식의 approach를 하면 될 것으로 생각됩니다. 내시경적 치료가 성공적인지 여부는 대부분 24시간 이내에 판단됩니다. 하루 밤을 보내면서 발열이 없고 통증이 경미해지면 수술이 필요없는 경우이며, 심한 통증이 지속되면 아무리 내시경적으로 완전하게 치료를 하였다고 하더라도 심각하게 수술적 치료를 고려하여야 합니다. [2004-12]
그림과 같이 시술 도중에 육안적으로 관찰되는 frank perforation이 있는 경우에는 내시경적 치료의 적응증이 됩니다. 대부분의 경우 clip을 이용하여 perforation을 직접 closure하면 수술적 치료 없이 호전되는 경우가 많습니다. 이처럼 내시경적 치료를 시행한 frank perforation에서 언제 diet를 시작하여야 하는가에 대한 정해진 원칙은 없으나 앞서 언급한 microperforation과 동일한 방식의 approach를 하면 될 것으로 생각됩니다. 내시경적 치료가 성공적인지 여부는 대부분 24시간 이내에 판단됩니다. 하루 밤을 보내면서 발열이 없고 통증이 경미해지면 수술이 필요없는 경우이며, 심한 통증이 지속되면 아무리 내시경적으로 완전하게 치료를 하였다고 하더라도 심각하게 수술적 치료를 고려하여야 합니다. [2004-12]
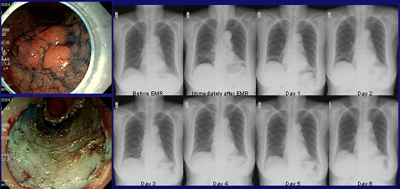 조기위암이나 위선종의 내시경적 치료에는 항상 출혈과 천공의 위험성이 따릅니다. 전통적으로 사용되던 inject and cut 혹은 inject, lift and cut 방법에 비하여 needle knife, IT knife, Flex knife, hook knife 등 도구를 이용한 광범위한 위점막절제술은 출혈과 천공의 위험성이 다소 높습니다. 합병증이 발생된 경우 과거에는 수술에 의존하는 경우가 많았으나 최근에는 내시경을 이용하여 치료하는 경우가 대부분입니다. 특히 위점막절제술과 연관된 대부분의 천공은 내시경적 방법과 금식, nasogastric tube, IV antibiotics 등 내과적 치료로 해결할 수 있습니다. 내시경 시술 도중 perforation이 발견되면 clip을 이용하여 즉시 closure를 하는 것이 좋으며 내시경적으로 직접 closure 하기 어려운 경우에는 omental patch를 이용하여 closure 하기도 합니다. 그러나 상당수의 천공은 시술 도중 발견되지 않고 시술 직후 시행한 chest X-ray에서 발견이 되며, 이 경우 복강내로 들어간 공기의 양이 상당히 많을 수 있습니다. 이는 시술 도중에 눈에 보이지 않은 매우 작은 천공이 발생하였으나 지속적으로 공기를 주입하면서 시술을 하였기 때문인데 저는 이러한 경우를 microperforation으로 부르고 있습니다. 저는 microperforation 발견된 경우에 내시경검사를 다시 시행할 필요는 없다고 생각합니다. 눈으로 보이는 perforation이 있어 내시경적으로 repair를 한 예와 및 microperforation 모두에서 천공 발생 후 금식, nasogastric tube, IV antibiotics를 통하여 더 이상 악화되지 않고 수술을 필요로 하지 않고 호전되는 예가 많습니다. 복강내 공기가 너무 많으면 주사기를 이용하여 공기를 빼 주면 환자의 복통이 보다 빠른 속도로 호전됩니다.
조기위암이나 위선종의 내시경적 치료에는 항상 출혈과 천공의 위험성이 따릅니다. 전통적으로 사용되던 inject and cut 혹은 inject, lift and cut 방법에 비하여 needle knife, IT knife, Flex knife, hook knife 등 도구를 이용한 광범위한 위점막절제술은 출혈과 천공의 위험성이 다소 높습니다. 합병증이 발생된 경우 과거에는 수술에 의존하는 경우가 많았으나 최근에는 내시경을 이용하여 치료하는 경우가 대부분입니다. 특히 위점막절제술과 연관된 대부분의 천공은 내시경적 방법과 금식, nasogastric tube, IV antibiotics 등 내과적 치료로 해결할 수 있습니다. 내시경 시술 도중 perforation이 발견되면 clip을 이용하여 즉시 closure를 하는 것이 좋으며 내시경적으로 직접 closure 하기 어려운 경우에는 omental patch를 이용하여 closure 하기도 합니다. 그러나 상당수의 천공은 시술 도중 발견되지 않고 시술 직후 시행한 chest X-ray에서 발견이 되며, 이 경우 복강내로 들어간 공기의 양이 상당히 많을 수 있습니다. 이는 시술 도중에 눈에 보이지 않은 매우 작은 천공이 발생하였으나 지속적으로 공기를 주입하면서 시술을 하였기 때문인데 저는 이러한 경우를 microperforation으로 부르고 있습니다. 저는 microperforation 발견된 경우에 내시경검사를 다시 시행할 필요는 없다고 생각합니다. 눈으로 보이는 perforation이 있어 내시경적으로 repair를 한 예와 및 microperforation 모두에서 천공 발생 후 금식, nasogastric tube, IV antibiotics를 통하여 더 이상 악화되지 않고 수술을 필요로 하지 않고 호전되는 예가 많습니다. 복강내 공기가 너무 많으면 주사기를 이용하여 공기를 빼 주면 환자의 복통이 보다 빠른 속도로 호전됩니다.
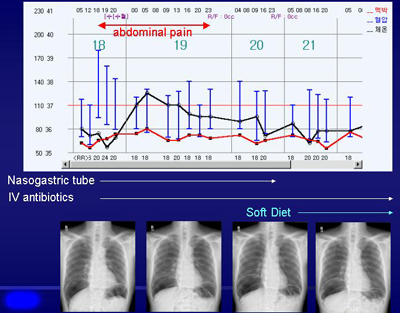 문제는 diet를 시작할 시점을 정하는 것입니다. 저는 환자의 통증과 압통이 좋아지고, 혈액검사에서 WBC count가 감소하고, 발열이 없으면 통상 시술 3일 후에 Soft diet를 시작합니다. 그 전날 물만 드시게 하는 경우도 있습니다. 환자의 증상이 좋아지고 있는 상황에서 diet를 시작하기 전 UGI series를 다시 시행할 필요는 거의 없는 것으로 생각됩니다. 복강내 공기가 남아있다고하여 diet를 시작하지 못할 이유는 전혀 없습니다. perforating wound가 완전히 closure 되었다고 하더라도 복강내 공기가 없어지기까지는 수일에서 수주까지의 시간이 소요되기 때문입니다. 저는 시술 5주후에도 복강내 공기가 남아있는 경우를 경험하기도 하였습니다. 흉강과 달리 복강은 air exchange가 활발하게 이루어지기 어렵기 때문에 공기가 흡수되는데는 많은 시간이 소요된다고 생각됩니다. 그림에서 제시된 예는 gastric EMR 후 perforation이 발생하였을 때 복막염을 의심케하는 symptom과 sign이 없어진 경우에는 비록 복강내에 다량의 공기가 남아있다고 하더라도 diet를 시작할 수 있음을 보여주고 있습니다. [2004-4]
문제는 diet를 시작할 시점을 정하는 것입니다. 저는 환자의 통증과 압통이 좋아지고, 혈액검사에서 WBC count가 감소하고, 발열이 없으면 통상 시술 3일 후에 Soft diet를 시작합니다. 그 전날 물만 드시게 하는 경우도 있습니다. 환자의 증상이 좋아지고 있는 상황에서 diet를 시작하기 전 UGI series를 다시 시행할 필요는 거의 없는 것으로 생각됩니다. 복강내 공기가 남아있다고하여 diet를 시작하지 못할 이유는 전혀 없습니다. perforating wound가 완전히 closure 되었다고 하더라도 복강내 공기가 없어지기까지는 수일에서 수주까지의 시간이 소요되기 때문입니다. 저는 시술 5주후에도 복강내 공기가 남아있는 경우를 경험하기도 하였습니다. 흉강과 달리 복강은 air exchange가 활발하게 이루어지기 어렵기 때문에 공기가 흡수되는데는 많은 시간이 소요된다고 생각됩니다. 그림에서 제시된 예는 gastric EMR 후 perforation이 발생하였을 때 복막염을 의심케하는 symptom과 sign이 없어진 경우에는 비록 복강내에 다량의 공기가 남아있다고 하더라도 diet를 시작할 수 있음을 보여주고 있습니다. [2004-4]
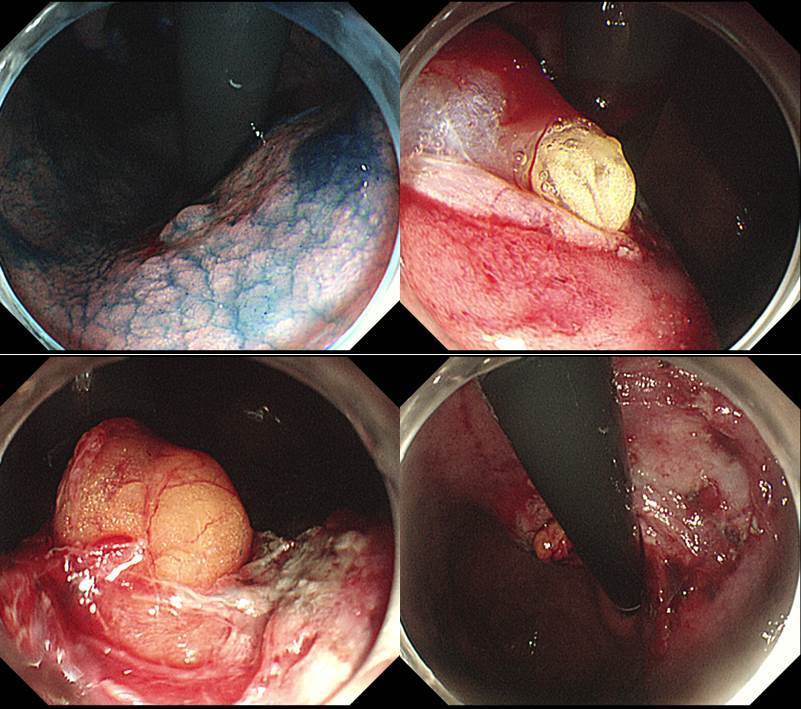 조기위암 ESD를 하는 도중 밝은 노란색이 보여서 천공인 줄 알고 깜짝 놀랐습니다. 그런데 자세히 보니 perforating hole이 없었습니다. 환자도 너무 stable하고. 그래서 끝까지 시술하였고 시술 후 X-ray도 정상이었습니다. Subcutaneous fat nodule이었습니다. 휴~~~ [2019-3]
조기위암 ESD를 하는 도중 밝은 노란색이 보여서 천공인 줄 알고 깜짝 놀랐습니다. 그런데 자세히 보니 perforating hole이 없었습니다. 환자도 너무 stable하고. 그래서 끝까지 시술하였고 시술 후 X-ray도 정상이었습니다. Subcutaneous fat nodule이었습니다. 휴~~~ [2019-3]
Non-lifting이 뚜렷하면 ESD를 중간에 중단할 수 있습니다. 그러나 ESD의 기술적 진보에 따라서 이제는 여간한 non-lifting에서도 ESD를 시행하는 것은 가능합니다. 단지 시술 후 병리 결과가 좋지 않아서 수술할 확률이 높을 뿐입니다.
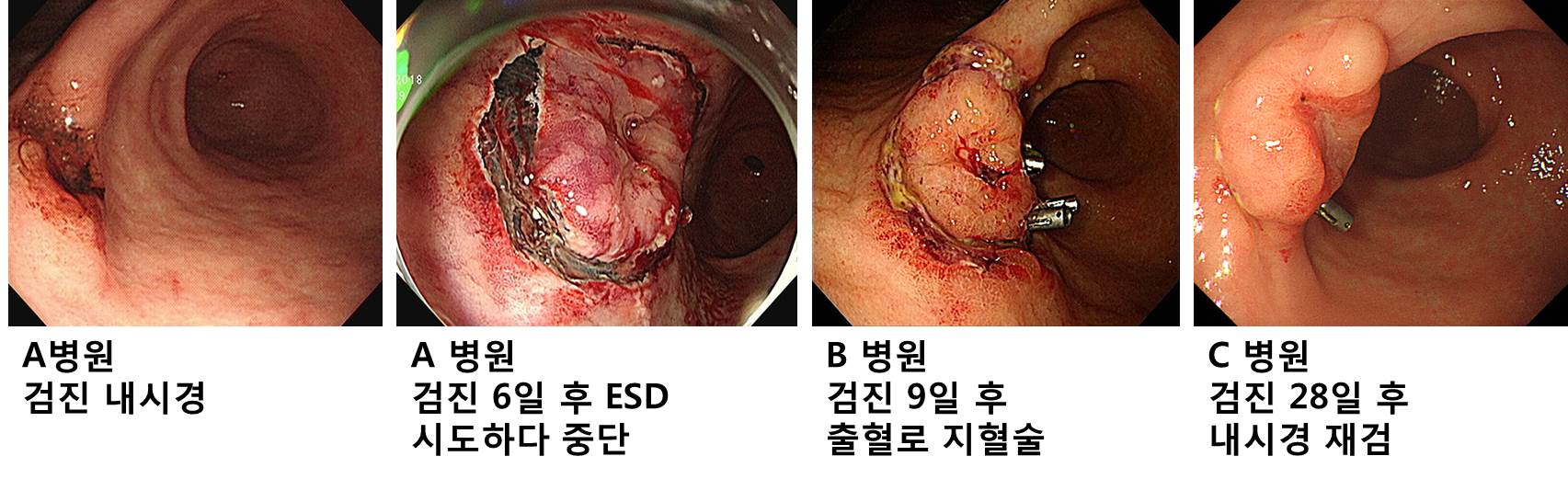 Non-lifting으로 시술을 중단하였고, 출혈하였고, 지혈술 받으셨고, 제2의 병원 응급실 경유, 제3의 병원에서 검사를 받고 수술까지 받게 된 환자 [2017]
Non-lifting으로 시술을 중단하였고, 출혈하였고, 지혈술 받으셨고, 제2의 병원 응급실 경유, 제3의 병원에서 검사를 받고 수술까지 받게 된 환자 [2017]
ESD 후 절제 표본을 잘 펼쳐서 고정해야 합니다. 줄맞춰 pin을 꽂아두면 약간 편리하기는 합니다. 이를 위해서 누군가는 귀찮은 일을 해야 합니다. 그래서 생각해 보았습니다. 꼭 pin을 세워야 할까요? 그냥 던져 놓으면 어떨까요? 별 차이가 없었습니다. 앞으로 pin을 세우지 말라고 지시하였습니다. 다들 좋아했습니다. [2018-9]

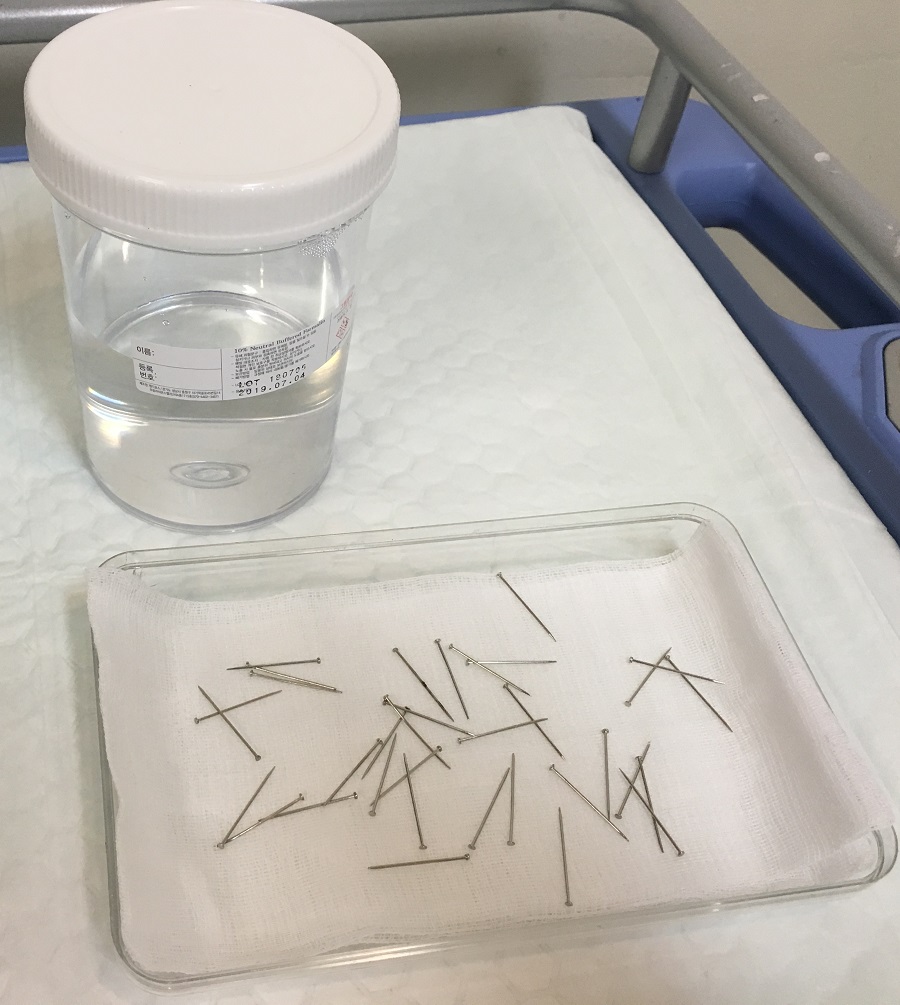 좌측: 과거(2018년 8월까지)의 방식. 우측: 현재의 방식. 이렇게 대강 던져놓아도 핀을 집어 표본을 고정하는데 불편함이 없었습니다. 간호사들의 잡무를 줄여주는 것도 중요한 일입니다. 잡무가 줄어들면 보다 본질적인 업무에 집중할 수 있기 때문입니다.
좌측: 과거(2018년 8월까지)의 방식. 우측: 현재의 방식. 이렇게 대강 던져놓아도 핀을 집어 표본을 고정하는데 불편함이 없었습니다. 간호사들의 잡무를 줄여주는 것도 중요한 일입니다. 잡무가 줄어들면 보다 본질적인 업무에 집중할 수 있기 때문입니다.
 EMR로 절제한 조직의 크기 및 병소의 크기를 기록하기 위하여 여러 종류의 도구를 사용할 수 있습니다. 흔히 절제된 조직을 핀으로 고정한 후 내시경을 근접하여 촬영을 하는데, 이때 절제조직 바로 옆에 자를 놓고 사진을 찍어두는 경우가 많습니다. 일반적인 사무용 자는 눈금이 가늘기 때문에 내시경으로 사진을 찍어두면 잘 보이지 않는 경우가 많습니다. ESD를 시행하여 병소를 매우 크게 절제하고 사진을 찍으면 이러한 현상이 더욱 두드러집니다. 이러한 단점을 극복하지 위해서는 반사되지 않고 눈금이 진한 사무용 자를 구하여 사용하는 것이 좋습니다. 위 그림은 제가 사용하였던 여러가지 크기 측정 도구인데 최근에는 맨 우측의 다소 둔탁해 보이는 자를 사용하고 있습니다. 반사가 되지 않고 눈금이 가장 진하기 때문입니다. [2005-1-31] 최근에는 절제 표본 크기는 눈짐작으로 하고 있습니다. 병리과에서 정확히 측정해주기 때문에 내시경실에서 시간을 들여 mm 단위로 정확히 기록을 남길 필요는 없습니다. 의료제도 변화로 인하여 상급종합병원에 너무 많은 환자들이 몰려들고 있어서 아주 꼭 필요한 절차 이외에는 모두 생략하고 있습니다. 안타깝습니다. [2019-7-15]
EMR로 절제한 조직의 크기 및 병소의 크기를 기록하기 위하여 여러 종류의 도구를 사용할 수 있습니다. 흔히 절제된 조직을 핀으로 고정한 후 내시경을 근접하여 촬영을 하는데, 이때 절제조직 바로 옆에 자를 놓고 사진을 찍어두는 경우가 많습니다. 일반적인 사무용 자는 눈금이 가늘기 때문에 내시경으로 사진을 찍어두면 잘 보이지 않는 경우가 많습니다. ESD를 시행하여 병소를 매우 크게 절제하고 사진을 찍으면 이러한 현상이 더욱 두드러집니다. 이러한 단점을 극복하지 위해서는 반사되지 않고 눈금이 진한 사무용 자를 구하여 사용하는 것이 좋습니다. 위 그림은 제가 사용하였던 여러가지 크기 측정 도구인데 최근에는 맨 우측의 다소 둔탁해 보이는 자를 사용하고 있습니다. 반사가 되지 않고 눈금이 가장 진하기 때문입니다. [2005-1-31] 최근에는 절제 표본 크기는 눈짐작으로 하고 있습니다. 병리과에서 정확히 측정해주기 때문에 내시경실에서 시간을 들여 mm 단위로 정확히 기록을 남길 필요는 없습니다. 의료제도 변화로 인하여 상급종합병원에 너무 많은 환자들이 몰려들고 있어서 아주 꼭 필요한 절차 이외에는 모두 생략하고 있습니다. 안타깝습니다. [2019-7-15]
 ESD로 절제된 조직은 pin으로 잘 펴서 고정을 해야만 병리학적 완전절제여부를 확인할 수 있습니다. 하단 첫번째 그림은 절제된 조직의 아래쪽 사진이며 하단 두번째 그림은 진주핀을 이용하여 고정한 모습니다. 일반 사무용 핀에 비하여 진주핀이 가늘기 때문에 조직손상이 적어서 과거에는 사용하였으나 최근에는 통상의 사무용 핀을 쓰고 있습니다. 제단용으로 사용하는 보다 가는 핀이 있지만 구하기가 쉽지 않습니다. 고정 후 indigocarmine을 살포하고 근접사진을 찍어두면 도움이 되지만 최근에는 귀찮아서 그냥 사진만 찍고 있습니다. [2004-11-12, Update: 2019-7-20]
ESD로 절제된 조직은 pin으로 잘 펴서 고정을 해야만 병리학적 완전절제여부를 확인할 수 있습니다. 하단 첫번째 그림은 절제된 조직의 아래쪽 사진이며 하단 두번째 그림은 진주핀을 이용하여 고정한 모습니다. 일반 사무용 핀에 비하여 진주핀이 가늘기 때문에 조직손상이 적어서 과거에는 사용하였으나 최근에는 통상의 사무용 핀을 쓰고 있습니다. 제단용으로 사용하는 보다 가는 핀이 있지만 구하기가 쉽지 않습니다. 고정 후 indigocarmine을 살포하고 근접사진을 찍어두면 도움이 되지만 최근에는 귀찮아서 그냥 사진만 찍고 있습니다. [2004-11-12, Update: 2019-7-20]
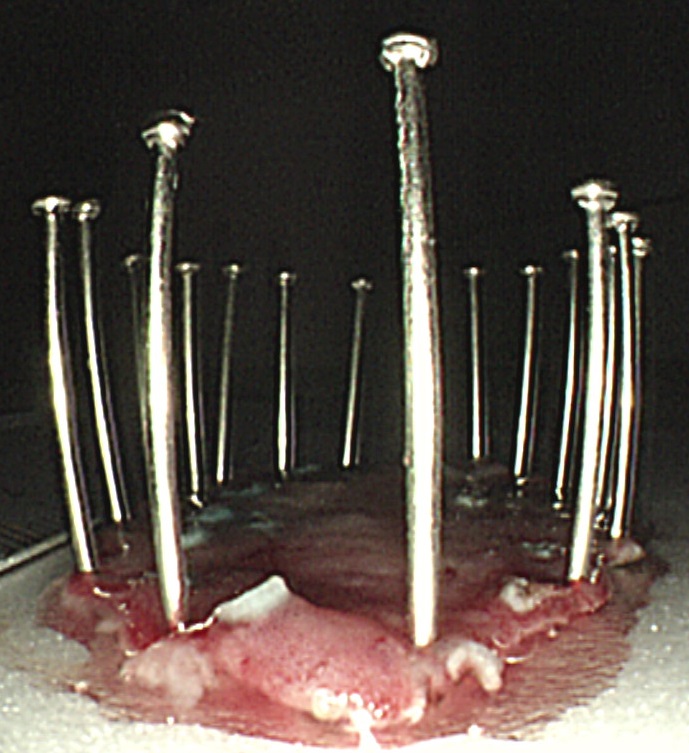
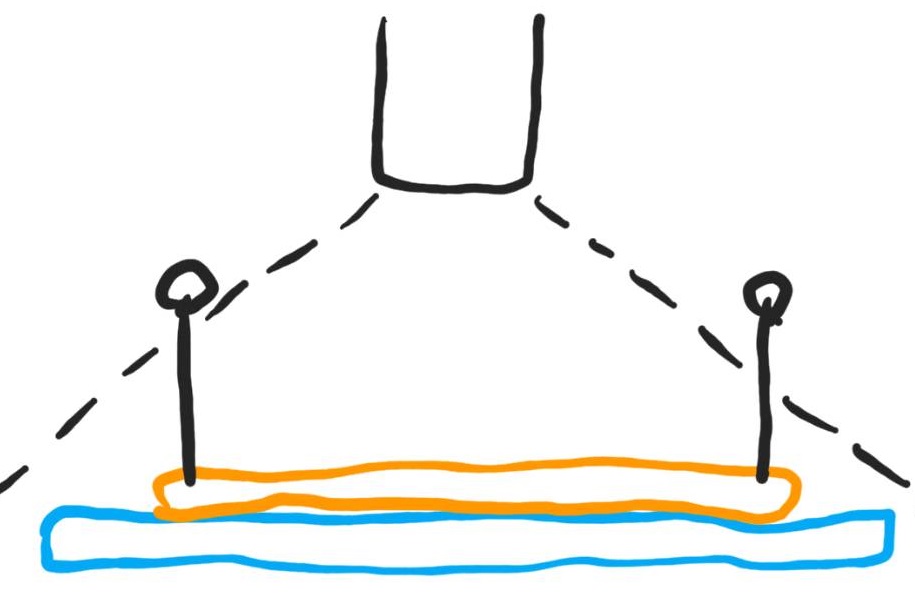 핀은 똑바로 꽂으면 됩니다. 핀을 똑바로 꽂아도 사진을 찍으면 핀이 벌어져 보입니다. 내시경은 광각렌즈이기 때문입니다. [2019-7-14]
핀은 똑바로 꽂으면 됩니다. 핀을 똑바로 꽂아도 사진을 찍으면 핀이 벌어져 보입니다. 내시경은 광각렌즈이기 때문입니다. [2019-7-14]

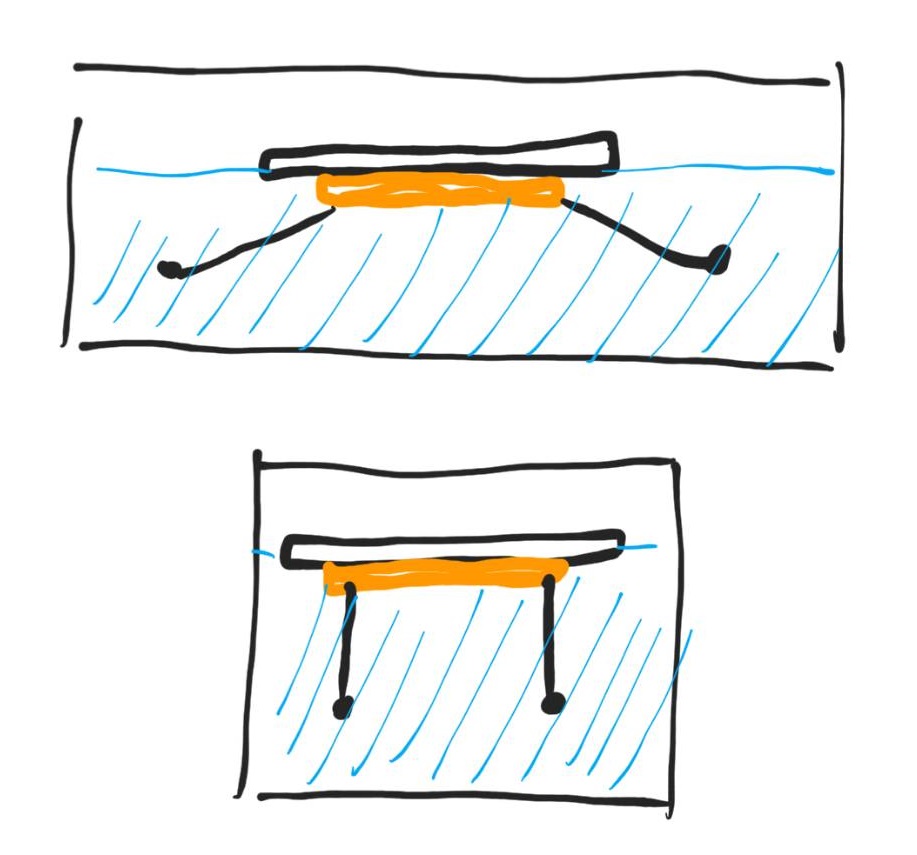 핀을 눕혀서 꽂으면 불필요하게 표본이 커져서 샘플 formalin 통 또한 큰 것을 써야 합니다. 핀은 똑바로 꽂읍시다. [2019-7-14]
핀을 눕혀서 꽂으면 불필요하게 표본이 커져서 샘플 formalin 통 또한 큰 것을 써야 합니다. 핀은 똑바로 꽂읍시다. [2019-7-14]
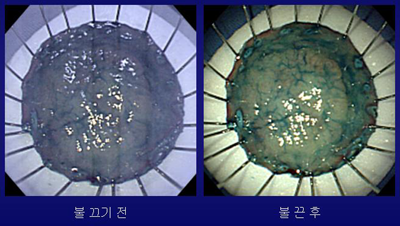 ESD 조직의 사진을 찍을 때 주변을 어둡게 해 주어야만 사진이 선명하게 나옵니다. [2004-1-11]
ESD 조직의 사진을 찍을 때 주변을 어둡게 해 주어야만 사진이 선명하게 나옵니다. [2004-1-11]
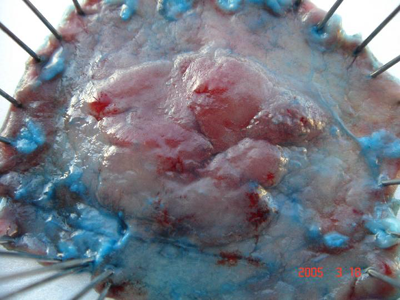 주변을 어둡게 하고 내시경을 이용하여 고정한 표면을 촬영하여도 비교적 볼 만한 사진을 얻을 수 있습니다. 그러나 내시경의 렌즈는 상당한 광각렌즈이므로 barrel distortion이 발생합니다. 바깥 쪽으로 갈수록 영상이 심하게 왜곡된다는 뜻입니다. 이를 극복하기 위하여 밝은 자연광하에서 강력한 접사능력이 있는 digital camera로 근접 촬영을 하면 왜곡 없는 선명한 영상을 얻을 수 있습니다. 저는 일반적인 아마추어용 digital camera 중에서 1 cm까지 접사가 가능한 model (DSC-T3)을 이용하여 EMR 절제 표본을 찍고 있습니다. 위 그림은 mucosa에 국한된 2.5 cm 크기의 융기형 조기위암을 절제한 표본을 촬영한 예입니다. [2005-4-1]
주변을 어둡게 하고 내시경을 이용하여 고정한 표면을 촬영하여도 비교적 볼 만한 사진을 얻을 수 있습니다. 그러나 내시경의 렌즈는 상당한 광각렌즈이므로 barrel distortion이 발생합니다. 바깥 쪽으로 갈수록 영상이 심하게 왜곡된다는 뜻입니다. 이를 극복하기 위하여 밝은 자연광하에서 강력한 접사능력이 있는 digital camera로 근접 촬영을 하면 왜곡 없는 선명한 영상을 얻을 수 있습니다. 저는 일반적인 아마추어용 digital camera 중에서 1 cm까지 접사가 가능한 model (DSC-T3)을 이용하여 EMR 절제 표본을 찍고 있습니다. 위 그림은 mucosa에 국한된 2.5 cm 크기의 융기형 조기위암을 절제한 표본을 촬영한 예입니다. [2005-4-1]
 2019년 5월 22일 '생로병사의 비밀'에서 소개된 장면. 아산병원 정훈용 교수님께서는 ESD 표본을 예쁘게 고정한 후 i-Pad로 촬영한 사진을 환자의 가족들에게 보여드리면서 설명하신다고 합니다. [2019-7-14]
2019년 5월 22일 '생로병사의 비밀'에서 소개된 장면. 아산병원 정훈용 교수님께서는 ESD 표본을 예쁘게 고정한 후 i-Pad로 촬영한 사진을 환자의 가족들에게 보여드리면서 설명하신다고 합니다. [2019-7-14]

EMR, ESD를 시행하고 난 후 정확한 시술 과정을 기록하여 두는 것이 좋습니다. 저는 (1) 병변의 특성을 기술하고, (2) 시술과정을 간략하게 요약하고, (3) 시술에 사용된 주된 도구를 기록하고, (4) 합병증 발생의 유무를 기록하고, (5) 전체적인 결론을 맺은 후, (6) 환자 관리에 대한 추천을 적는 방식을 택하고 있습니다. 긴 기술을 하고 난 후에는 이에 따른 기록도 자세히 남겨두는 것이 좋다고 생각합니다. [2004. 11.]
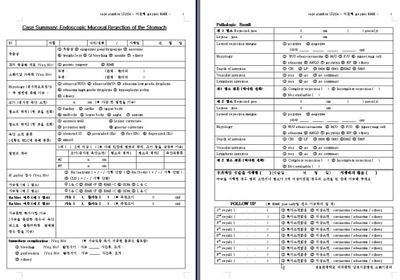
병원 의무기록 이외에 간략하게 입력할 수 있는 형태로 case summary form을 작성하여 시술과정을 요약하고 병리결과를 기록하고 추적관찰 결과를 확인하도록 하고 있습니다. 이 형태는 환자의 의무기록에는 들어가지 않고 개인적으로 자료 정리에 이용하고 있습니다. [2004. 11. 17]
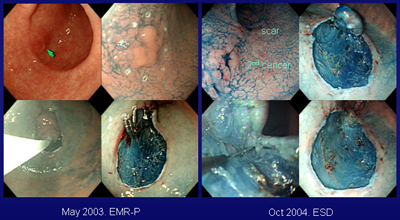
위암의 내시경적 치료 후 follow up schedule은 기관마다 차이가 있습니다. 저는 시술 후 첫 내시경을 시술 3개월 후에 시행하고 있습니다. 위암의 내시경 치료 후 가장 큰 골치거리는 metachronous cancer입니다. 대부분의 metachronous cancer는 내시경으로 절제할 수 있는 조기에 발견되므로 치료부위만을 관찰할 것이 아니고 위점막 전체를 자세히 관찰하여 적극적으로 second cancer를 찾으려는 노력이 필요합니다. 본 case는 원 병소에 매우 가까운 부분에서 발견된 second cancer로 ESD를 이용하여 치료하였습니다. 원 병소에 가까운 부분이기 때문에 submucosal fibrosis가 있었으나 needle knife를 이용한 direct cutting 방법으로 해결을 하였습니다. [2005. 2. 1]
[EMR/ESD 후 융기형 반흔]
EMR로 인한 artificial ulcer는 대부분 benign gastric ulcer scar와 비슷하게 healing이 되지만 일부에서는 protruded lesion의 모양을 띄는 경우가 있습니다. 2001년 대한위암학회지에 실린 보고를 보면 (대한위암학회지 2001;1:55-59) EMR scar의 약 15%에서 protruded lesion이 발생하며 조직검사에서는 장상피화생 또는 재생성 과형성증을 보였고, 따라서 원발병변의 재발과는 무관한 양성 병변으로 정상 주위점막의 과형성능의 발현인 경우가 많다는 결론이었습니다. EMR의 경험이 많지 않은 단계에서는 시술 3-6개월 후 follow up 내시경에서 protruded lesion을 보고 재발을 의심하는 것이 당연하겠습니다. 그러나, 첫 시술에서 complete resection을 보였다면 반년 정도의 follow up 기간에 재발성 병소가 protruded mass로 나오는 경우는 거의 없다는 것이 저의 짧은 경험입니다. 조직소견은 일반적인 hyperplastic polyp과 매우 유사한 것 같습니다. [2005. 2. 15.]
[2018-9-5. Question from a friend in Mongo]
How are you sensei! I have a question about this case. 56 y/o male patient underwent ESD 9 months ago. Pathology: Tubular adenocarcinoma Mod diff Confined LP, pT1aNx,Mx.
Now, Endoscopy revealed elevated growth on ESD base. Biopsy result was: hyperplastic growth. Is it possible? Please see the attached picture after ESD growth.
[2018-9-5. 이준행 답변]
Most of EMR/ESD-induced ulcers heal completely just like benign gastric ulcer. However, some cases heal like hyperplastic polyps. According to an old Korean report, 15% of EMR scars heal as a protruded lesion. . Pathology for this protruded lesion is usually intestinal metaplasia or hyperplastic polyp. Gastric cancer after ESD may locally recur, but it takes time. Protruded lesion at ESD site within a year or two is mostly benign. I am glad to get further question from you anytime.
[2014-11-7. 애독자 질문]
EGC나 dysplasia로 ESD한 환자에서 f/u시 routine으로 그 병변에서 biopsy를 하는 것 같습니다. routine Bx가 맞는 것인지, recurrence가 의심되는 경우에만 하는 것인지 궁금합니다.
[2015-12-21. 이준행 답변]
여러 선생님들의 의견을 모아서 답변드린다는 것이 벌써 1년이 되었습니다. 죄송합니다. 그런데 아직 정확한 답변을 만들지 못했습니다. 대부분 local recurrence는 병리학적 incomplete resection 환자에서 발생하지만 (국소재발 증례), 드물게 병리학적 complete resection 환자에서 발견되기도 합니다. 따라서 병리학적 complete resection이라는 이유로 조직검사를 하지 말라고 답하기 어렵습니다. ESD 후 국소 재발은 매우 드물고 대부분 metachronous recur 혹은 extragastric recur가 문제가 됩니다. 사실 local recur는 조금 늦게 발견되어도 큰 문제가 없습니다. 그래서 육안적으로 재발이 의심될 때만 조직검사를 하도록 권하는 의사도 있습니다.
ESD 시술자가 직접 추적내시경을 못하는 경우도 많고, 지금까지의 local recur가 육안적으로 재발이 의심되지 않은 경우도 많았다는 점을 고려해야 할 것 같습니다. 따라서 저는 ESD 후 3년 정도는 항상 조직검사를 하도록 권하고 싶습니다. 그 이후는 육안소견에 이상이 없으면 조직검사를 하지 않아도 좋다고 생각합니다. (물론 개인의견입니다. 교수님마다 생각이 다를 수 있습니다. Consensus를 만들기 어려웠습니다.)
 ESD 후 추적검사에서 Helicobacter에 대하여?
ESD 후 추적검사에서 Helicobacter에 대하여?
[2014-11-7. 애독자 질문]
ESD 후 추적관찰 환자에서 조직검사 결과를 확인하다가 보면 H. pylori 양성, 음성이 반복되기도 합니다. H. pylori 양성이라 제균치료 후 음전되었다가 재감염이 되었을 거라 해석을 하고 있기는 하지만, Bx는 특정부위만 검사를 하는 것이다 보니 실제로는 제균치료가 되지 않았음에도 위음성이 나온 것을 배제할 수 없을 것 같습니다. 그래서 질문입니다. 제균치료 후 biopsy가 아닌 UBT검사를 하는 것이 더 정확할까요? 음전 후 다시 양성으로 나온 경우 1차 치료를 해야할지 2차 치료를 해야할지 궁금합니다.
[2015-12-21. 이준행 답변]
ESD 후 헬리코박터 제균치료에 대한 논문의 연구방법에 문제가 발견되곤 합니다. 즉 H. pylori를 체계적으로 검사하지 않았다는 것입니다. 정해진 원칙대로 H. pylori를 검사하지 않고 (즉 병소 scar에서 H. pylori 여부만 본 경우가 많습니다) 어떻게 H. pylori를 논할 수 있겠습니까?
ESD 후에는 암의 재발에 온통 관심이 쏠리기 때문에 H. pylori에 대한 체계적인 검사를 못하는 것입니다. 저는 위암 내시경치료 후 H. pylori가 나오면 일차제균치료를 하고 꼭 UBT를 처방하고 있습니다. 만약 음성으로 나왔다 다시 양성으로 나오는 경우, 그 간격이 1년을 넘었으면 초치료를 다시 하고 있습니다.
 일본 올림푸스에서 IT knife nano라는 새로운 제품을 선보였습니다.
일본 올림푸스에서 IT knife nano라는 새로운 제품을 선보였습니다.
국가에서 위암적정성 평가를 하고 있으며 관련하여 병원에서 자료를 모아 정기적으로 보고하고 있습니다.
2019년 monitoring. 수술이 필요하다고 나온 환자의 84%가 실제 수술을 받고 있습니다.
2019년 monitoring. 위암 ESD의 입원 진료비는 250여만원인데 대부분은 보험으로 cover되고 있습니다.
[2015-8-27. 애독자 질문]
Pylorus 7시 방향의 1cm raised erosion에서 조직검사상 tubular adenoma with low grade dysplasia 소견 보였습니다. EMR P 예정인데 pylorus 인접부위라 최대한 pylorus 쪽은 안 건드리려 하는데요, 최대한 enbloc resection을 시도하겠지만... 이런 경우 시술중 pylorus까지 incision이 들어갈 때 일부 논문에서 dexamethasone을 pylorus 점막에 주입하면 pylorus stricture를 줄일 수 있다고 본 것 같은데 이런 경우 선생님께서는 어떻게 시술하시는지요?
[2015-8-27. 이준행 답변]
좋은 질문 감사합니다. 이런 경우 저는 말발굽절개법(horseshoe precutting method)을 쓰고 있습니다. 병소가 pyloric ring에 걸려있으면 360도 circumferential precutting이 어렵습니다. 물론 위쪽에서 3/4 정도 precutting하고 십이지장에서 retroflection하여 나머지 1/4를 precutting하면 더 좋을 것입니다. 그러나 십이지장에서 retroflection하여 precutting을 한다는 것이 말같이 쉽지 않습니다. 위암이라면 다소 위험성이 있더라도 위와 십이지장 양쪽에서 접근하는 방법을 시도해 볼 수 있겠으나 선종에서 그러할 필요가 있을지 의문입니다.
저는 3/4정도 precutting하고 난 후 submucosal dissection을 충분히 하고 마지막을 snare cutting으로 마무리합니다. 간혹 distal쪽의 resection margin이 애매하면 APC ablation을 추가합니다. 병소가 작으면 submucosal dissection을 하지 않아도 됩니다. 요컨데 (1) 270도 precutting → (2) submucosal dissection → (3) 충분한 injection → (4) snare cutting → (5) (필요시) APC ablation 추가 순서로 시술하고 있습니다. 270도 정도 절제하는 방법은 horseshoe precutting method (말발굽절개법)라고 부릅니다. 그냥 제가 지은 이름입니다.
증례는 크기가 작으므로 사진과 같이 300도 정도 cutting한 후 snare resection하면 되겠습니다. Submucosal dissection을 조금 해주면 훨씬 깔끔하게 시술됩니다.
식도 ESD에서 intralesional triamcinolone 혹은 oral steroid가 협착을 줄인다지만 약간의 위험도 있습니다. Pyloric ring의 경우 절반 이상 cutting되지 않으면 symptomatic stenosis는 오지 않는 것 같습니다. 만약 약간의 stenosis가 오더라도 TTS balloon dilatation으로 쉽게 해결할 수 있습니다. 조심스럽게 precutting만 잘 한다면 steroid까지는 필요하지 않을 것 같습니다. 협착에 대해서는 esd_stricture.html를 참고하시기 바랍니다.
[2017-4-25. 애독자 질문]
선생님은 Dual knife를 이용한 시술을 많이 하고 계시는데요, Dual knife에서 'Dual'은 무슨 뜻인지요?
[2017-4-27. 경북대 전성우 교수님 답변]
Dual 이라고 이름 붙인건, 팁을 오픈했을때 절개/절제가 가능한 측면과 팁을 close했을 때 앞쪽으로 살짝 돌출된 팁으로 마킹이나 미세 절제가 가능한 측면, 이 두 가지를 가지고 붙인 것이라 합니다. 크게 임팩트 있는 이름은 아닌 것 같은데, 어쨌든 설명은 그렇다고 들었습니다.
[2019-1-9. 애독자 편지]
안녕하세요 교수님. 저는 지방의 한 대학병원에서 전임의 2년차 수련을 마지고 지방의 종합병원에서 봉직의 생활을 하고 있습니다. Endotoday 는 전임의 시절부터 매일 챙겨 보고 있습니다.
제가 일하는 곳이 지방 종합병원인 관계로 제가 할 만한 ESD case 가 그렇게 많지는 않으나 우연한 기회에 Finemedix H type knife를 사용할 기회가 있어서 ESD 초심자 입장에서 의견을 전달해 보고자 합니다. H type knife 가 Dual knife 형태라고 하고 있으나 실제 사용시 기존에 쓰던 Dual knife 처럼 끝에 ball 이 달려 있는 형태가 아니라 needle knife 형태인데 끝이 무딘형태 입니다. 기존 dual knife 가 소문자 i 위에 점이 있다고 보면 H knife 는 I 같은 형태라고 보시면 되겠습니다. 이에 따른 시술 차이가 크지는 않으나 marking 할때 기존 Dual knife 보다는 좀 엷게(?) 된다고 해야되나요 이러한 차이가 있었습니다.
이상 ESD 초심자 의견이었습니다. 늦었지만 새해 복 많이 받으시고 건강하세요.
[2019-1-9. 이준행 답변]
좋은 의견 주셔서 감사합니다.
저는 Dual knife만을 이용하여 ESD를 하는 환자가 60%, Dual knife + IT-2 knife로 시술하는 환자가 20%, Dual knife + snare (+/- IT-2 knife)로 시술하는 환자가 20% 정도입니다. 한 환자에서 한 개의 knife 사용을 권하는 깍쟁이 (?) 정부의 의견에 따라 Dual knife alone으로 시술하는 예가 많습니다. (저는 가급적 규정을 지킵니다. 착한 학생 mode) 문제는 Dual knife alone으로 하면 시간이 조금 더 걸린다는 것입니다. '빠른 내시경보다 바른 내시경'을 주장하고 있지만, 도구 사용에 제한이 있어 ESD 시술 시간이 오래 걸리는 것은 환자에게 나쁜 일입니다. 그래서 가끔 snare를 사용하여 시간 절약을 하고 있습니다.
Finemedix H-type knife는 끝이 뾰족한 needle과 insulated ball을 가진 needle을 합친 형태이므로 이론적으로는 이상적인 knife입니다. Finemedix 사에서는 "Ultimate ESD knife"라고 부르고 있습니다. 제 생각에는 ultimate는 아니고 near-ultimate 정도는 됩니다.^^ Very close 합니다. 시술하면서 느낀 점 몇 가지입니다.
Finemedix H-type knife를 이용한 ESD
1. 말씀하신 것처럼 marking 할때 기존 Dual knife 보다는 좀 엷게 되는 것 같습니다. Dual knife를 사용할 때에는 needle을 내지 않은 상태에서 점막에 접촉하고 Spray Coagulation을 통과시키면 둥글고 진한 marking이 만들어지는데 H-type에서는 경계가 불분명하고 다소 흐린 marking이 되었습니다. H-type의 I-tip needle을 조금 내민 상태에서 전류를 통과시켰더니 작고 분명한 marking이 되더군요.
2. 사양으로는 Dual knife도 2 mm, H-type도 2 mm 이지만 사용자 입장에서는 H-type의 I-tip needle이 조금 더 길게 느껴졌습니다. 약간 가늘기 때문인 것 같습니다. Dual knife는 작고 야무진 단도 같은 느낌이고, H-type의 I-tip은 펜싱 칼 같다고나 할까요?
3. H-type의 O-tip needle (IT-2 knife와 비슷한 것)은 매우 만족스러웠습니다. 약간 가는 것이 Olympus IT-2 knife 보다는 Olympus IT knife와 비슷한 느낌이었습니다. 우리나라에서는 IT-2 knife만 사용되고 classic한 IT knife는 거의 사용되지 않고 있지만, 일본에서는 아직도 간혹 classic IT-knife를 찾는 전문가가 있다고 합니다. Sharp하게 잘리는 느낌이 좋기 때문입니다. (사시미 칼 같은 느낌?)
4. I-tip과 O-tip을 매우 가늘게 만들다보니 내구성은 다소 떨어지는 것 같습니다. 처음에는 I-tip과 O-tip이 모두 잘 작동하였은데 시술이 끝나고 확인해보니 I-tip은 더 이상 작동하지 않았습니다. 아마도 가느다란 연결부가 끊어진 모양입니다. 시술에는 문제가 없었습니다. I-tip은 시술 초기에 사용하고 중간부터는 O-tip만 사용하기 때문입니다. 만약 한번에 여러 병소를 치료할 때에는 다소 문제가 될 수 있을 것 같습니다. 간호사들에게 어린 아이 다루듯 조금 더 부드럽게 조작하도록 부탁했습니다. 살살~~~
5. H-type knife는 water-jet 기능을 위한 irrigation port도 있습니다. 고압력 pump를 가지고 있지 않아서 사용하지 못했지만... 개인적으로는 water-jet 기능이 없어도 좋으니 I-Tip을 조금 더 굵고 튼튼하게 만들어보면 어떨까 생각되었습니다.
[2019-3-28. 이준행 독백]
ESD를 받은 환자인데 문득 자신이 받은 치료가 수술인지 시술인지 물어오신 분이 계셨습니다. 수술과 시술의 기준은 명확하지 않습니다. 차병원의 조주영 교수님께서는 수술로 설명하고 계십니다. 저는 구태여 하나를 선택하라면 시술이라고 말하는 편입니다. 어느 누가 옳은 것도 아닙니다. 그래서 "내시경점막하절제술(ESD)"이라는 말로 표현하고 있습니다. 박리술이라는 말은 느낌이 좋지 않아서 사용하지 않습니다. 왠지 인디언이 생각나서요.
말하자면 아래와 같습니다.
환자: 제가 받은 치료가 수술입니까? 시술입니까?
이준행 답변: 내시경점막하절제술(ESD)입니다. 수술과 시술의 정의는 명확하지 않습니다. 의사마다 다르게 표협합니다.
환자: 그래도 하나를 고른다면 수술입니까? 시술입니까?
이준행 답변: 내시경점막하절제술(ESD)입니다. 명확하지 않은 것 중 하나를 고르는 것은 아무 의미가 없습니다.
환자: 보험회사에 서류를 내야 하는데 수술입니까? 시술입니까?
이준행 답변: 보험회사에 낼 서류라면 더더욱 하나를 고를 수 없습니다. 그냥 "내시경점막하절제술(ESD)"이라고 하는 것이 가장 정확합니다. "내시경치료"라고 해도 좋습니다 .
계속 반복...한 환자분께 설명해 드린 내용을 옮깁니다.
사보험이 우리나라 환자의 건강에 도움이 된다고 생각하지 않습니다. 환자들의 경제적 사정에 도움이 된다고 생각하지 않습니다. 바쁜 외래 시간에 얼토당토 없는 일로 환자와 다투는 일이 많아져서 정말 힘듭니다.
[2020-1-6. 이준행] 이런 저런 것을 물어보는 분이 많습니다. 상식에 준하면 된다고 답하고 있습니다.
[2020-11-11. 애독자 질문]
고령의 수술이 어려운 환자에서 lateral margin +시 ablation 외 도넛 모양으로 ESD를 추가 시행하는 경우는 없는지요?
[2020-11-11. 이준행 답변]
ESD는 수술이 필요한 합병증이 발생할 수 있는 시술로 수술의 definite contraindication인 환자는 ESD의 definite contraindication입니다. 수술의 relative indication이고 환자가 치료에 대한 적극적인 의사가 있고 가족들이 동의하면 조심스럽게 ESD를 시도해 볼 수 있습니다. 그러나 lateral margin positivity에 대한 additional ESD는 상당히 어렵고 합병증 우려가 높은 술기이므로 다시 한번 치료가 필요할지 논의가 필요합니다. 요컨데 가능하지만 가급적 피하는 것이 환자를 위해 좋다고 말씀드리고 싶고 저는 단 한번도 수술의 contra-indication인 환자에서 additional ESD를 해 본 적이 없습니다. 하지 않고 있습니다.
[2021-6-17] ERBE APC probe 관련 회사 직원의 편지
다름이 아니오라 APC (아르곤장비) 를 납품하던중 저희는 1회용 프루브(1회용이지만 대부분 재사용중입니다.) 만 나와서 재사용용 프루브는 공급이 안되다 보니 납품을 못하게되어 장비를 내시경실에 두고왔습니다.
재사용용 프루브에서 일회용프루브로 바뀌어 공급된다고는 사실 3년전부터 내시경실에 말씀드려왔습니다. 그전에도 아르곤 프루브는 삼성에서 사용량이 많지 않았습니다.(1년에 10개미만으로 납품했었습니다.) 그리고 워낙 출혈이 많지않게 시술하시고 아르곤프루브 말고도 지혈포셉등으로 지혈하기 때문일거라 생각합니다.
저희 ERBE 장비는 3년전부터 일회용프루브만 연결되도록 생산되어 납품하고 있습니다. 단 기존장비에 일회용 프루브를 사용하기 위해 장비의 소켓을 무상으로 교체해드려왔습니다. 극히 일부병원에서만 ERBE 장비에 BOWA 케이블 이용하여 BOWA 재사용용 프루 브를 사용중입니다. 6월에 심평원에서 정액수가로서 사용되는 ARGON PROBE 의 실태조사가 있었습니다. 향후 일회용품인 프루브의 현실적인 치료재료 수가가 정해질수도 있는 상황입니다.
두서없이 현재 상황을 설명드리게 되는점을 송구스럽게 생각합니다. 교수님. 회의에 참고하십사 하고 메일로 인사 드립니다.
이 환자를 ESD를 해야 할까요 - 시술 전 환자 선택 및 병기 설정을 중심으로 부산대학교 김광하. 2021년 내시경세미나 (log-in 필요)
Gastric ESD 아산병원 김도훈. 2021년 내시경세미나 (log-in 필요)
고위험 환자의 ESD, 주의하고 준비해야 할 점은? - 기저질환 및 복용약물 고려 가톨릭의대 박재명. 내시경세미나 (log-in 필요)
ESD를 위한 기기의 이해와 운용방법 연세대학교 윤영훈. 2017년 내시경세미나 (log-in 필요)
병변 위치에 따른 부위별 공략법 부산대학교 김광하. 2018년 내시경세미나 (log-in 필요)
Re-ESD for locally recurrent / incompletely resected gastric lesion with fibrosis 연세대학교 윤영훈. 2021년 내시경세미나 (log-in 필요)
위 ESD 배우기- 나의 좌충우돌 제주대학교 나수영. 2016년 내시경세미나 (log-in 필요)
2022-31. ESD 소개. ESD knife와 ESU를 중심으로.
[2022-9-8] Submucosal injection fluid 현황
3) 조기위암 내시경치료 이혁 교수님 인터뷰 (2022-3-31. 삼성서울병원 블로그)
© 일원내시경교실 바른내시경연구소 이준행. EndoTODAY Endoscopy Learning Center. Lee Jun Haeng.